[한국 바이오 글로벌 도전기]'유전자 치료'가 화두…헬릭스미스도 주목①노바티스 SMA 치료제, 주사 한번에 25억…CAR-T 등도 관심
필라델피아(미국)=민경문 기자공개 2019-06-13 08:07:25
[편집자주]
한국 바이오사업은 글로벌 빅파마와 비교하면 걸음마 단계다. 글로벌 빅파마들은 100년이 넘는 역사와 수십조원의 몸값을 자랑한다. 이제 막 신약 1~2개를 도전하는 벤처와 수십개의 오리지널 의약품을 보유한 빅파마를 비교하긴 힘들다. 하지만 한국 바이오 벤처들은 빠른 실행력과 틈새 시장 도전을 통해 경쟁력을 키워가고 있다. 미국 필라델피아에서 열린 바이오USA에서 만난 바이오벤처들의 목소리를 통해 한국 바이오 벤처의 현 주소와 글로벌 시장 도전기를 정리해본다.
이 기사는 2019년 06월 12일 07:30 thebell 에 표출된 기사입니다.
올해 BIO 인터내셔널 컨벤션(바이오 USA)를 관통한 헬스케어 트렌드는 무엇이었을까. '신상' 스마트폰이 매년 나오는 것처럼 의학 기술이 업데이트되는 건 아니지만 임상 진행과 적응증 확대 등을 둘러싼 변화들은 시장의 이목을 끌기 충분하다. 선진국과 일정 수준의 시간차(TIME LAG)가 있다는 점을 고려하면 향후 국내 바이오업계의 기술 흐름을 점쳐볼 기회이기도 하다.지난주 필라델피아에서 열린 바이오 USA는 부스 행사와 함께 다양한 스터디 섹션과 전문가 강의로 눈길을 끌었다. 그 중에서도 면역항암제에 대한 관심은 압도적이었다. 개별 회사 발표만 보더라도 면역항암제 관련 내용이 가장 많았다. 국내에서도 파멥신, 유틸렉스 등이 컴퍼니 PT를 선보였다.
앞서 열린 ASCO(미국임상종양학회)에서도 면역관문억제제와의 병용치료가 핵심 이슈였다. 벤처캐피탈 관계자는 "면역항암제 표적 타깃의 경우 PD-1 뿐만 아니라 백신, 항원보강제(Adjuvant), 세포치료제 등 다양하게 주목받고 있다"며 "최근에는 유전자 치료(Gene theraphy가 각광을 받고 있는 듯 하다"고 말했다.
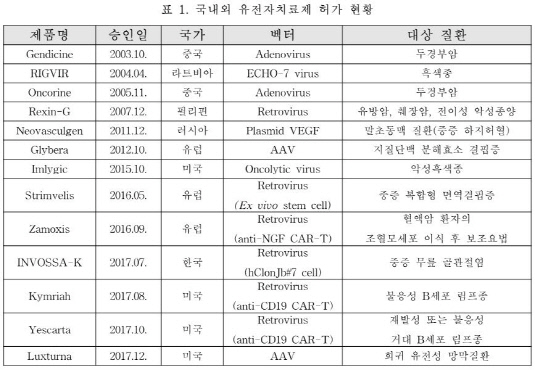
생명공학정책연구센터는 유전자치료제 시장이 2016년 5억8000만달러에서 2023년 44억200만달러 규모로 성장한다고 예상했다. 미국 재생의료 협의회(ARM)도 올해 1분기 372건의 유전자치료제 관련 임상이 진행중이라고 밝혔다. 이는 전년동기 대비 17% 증가한 수치다. FDA는 2025년까지 매년 20~25개의 새로운 세포·유전자치료제가 허가를 받을 것으로 전망했다.
|
유전자 치료는 희귀 질병에 효과를 보이고 있으나 복잡한 기술, 대량생산의 어려움 때문에 약가가 높다. 특히 바이오 USA 행사를 앞둔 5월 말 FDA로부터 승인 받은 노바티스의 SMA 치료제 '졸겐스마(Zolgensma)'는 단연 화제였다. 주사 치료 한번에 들어가는 비용은 25억원(210만 달러)에 달했다.
SMA(Spinal muscular atrophy)는 척수와 뇌간의 운동신경세포가 손상돼 점차 근육도 위축되는 신경근육계 유전질환이다. 노바티스는 지난해 4월 유전자치료제 개발기업 아벡시스를 87억달러(10조3000억원)에 인수한 바 있다. MSD의 케네스 프레이저 회장도 바이오 USA 슈퍼세션에서 발표자로 나서 유전자 치료제의 향후 잠재력을 강조했다.
국내에서는 헬릭스미스로 사명을 바꾼 바이로메드가 유전자 치료제 분야의 선두주자다. VM-202(당뇨병성신경병증)의 미국 3상을 진행하고 있으며 10월쯤 임상 결과 발표가 기대되고 있다. 이밖에 GC녹십자가 유전자재조합 혈우병 치료제 '그린진에프'의 중국 품목 허가를 신청하기도 했다.
한 미국 바이오회사 연구원은 "유전자 치료 개발은 최근 유전자 가위(크리스퍼)에 대한 연구가 급속도로 진전되고 있는 것과도 무관치 않을 것"이라며 "안전성에 대한 데이타가 좀더 축적될 경우 멀지 않은 시간에 상용화가 가능할 것으로 보인다"고 말했다.
CAR-T 역시 큰 틀에서는 유전자 치료제로 분류된다. 혈액 내에 존재하는T 세포를 분리해 여기에 특별한 유전자 (CAR)를 도입하고 이들이 특정 암들을 공격하는 구조다. FDA는 2017년과 2018년에 대표적인 CAR-T 치료제인 킴리아와 예스카타를 잇따라 승인한 바 있다.
|
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
best clicks
최신뉴스 in 전체기사
-
- 스튜디오산타클로스ENT, 주주권익 보호 '구슬땀'
- 이에이트, AI 시뮬레이션·디지털 트윈 기술 선보여
- MBK, '몸값 2조' 지오영 인수 SPA 체결 임박
- [2024 더벨 글로벌 투자 로드쇼-베트남]한인이 설립한 RCE, 세계 첫 ‘중장비 온라인 중고거래’
- 회계법인 해솔, 부동산 타당성 자문 업무협약
- [2024 더벨 글로벌 투자 로드쇼-베트남]베트남의 지오영 '바이메드'·전기오토바이 '셀렉스' 눈길
- 지아이에스, 코스닥 상장 위한 예비심사신청서 제출
- [꿈틀대는 토큰증권 시장]'업계 표준' 루센트블록, '두자릿수' 레코드 조준
- [Company & IB]조달 '막바지' 롯데그룹, 롯데케미칼에 쏠리는 눈
- '910억 CB 발행' 아스트, 경영 정상화 속도 낸다