렉라자의 질주, 비용에서 자산으로...개량신약 6종 임상 3상 유한양행 3년새 자산화한 개발비 35배↑, 레이저티닙 84% 비중
임정요 기자공개 2023-04-21 07:06:29
[편집자주]
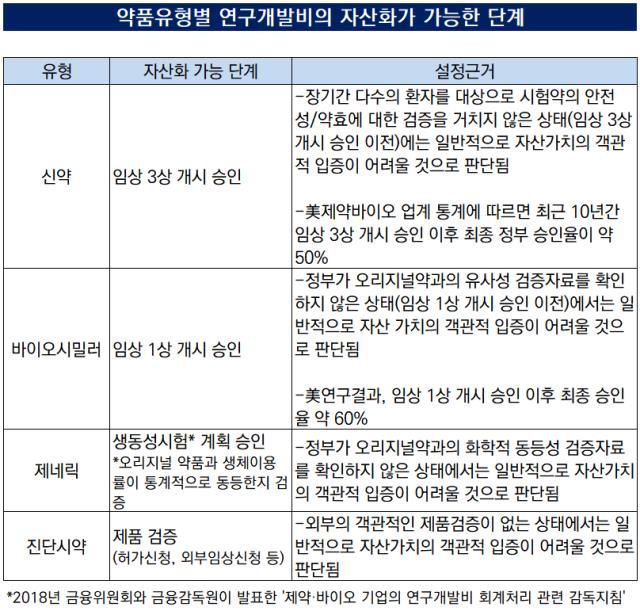
2018년 금융감독원이 발표한 지침에 따라 신약개발사들은 임상 3상 단계 이상의 파이프라인만 무형자산으로 인식할 수 있다. 바이오시밀러의 경우 임상 1상 개시 단계부터 자산화가 가능하다. 연구개발비의 무분별한 자산화를 지양하고자 상업화 가능성이 가시화 되는 시점을 감안하는 지침이 생겼다. 제약사들이 자산화한 개발비 현황은 상업화 단계에 가까워진 파이프라인을 파악하는 수단일 뿐 아니라 그간 들여온 파이프라인별 R&D 비용을 파악할 수 있는 도구다. 더벨은 주요 제약사의 자산화한 개발비를 살펴 실현가능한 미래수익성을 따져보았다.
이 기사는 2023년 04월 21일 08:53 THE CFO에 표출된 기사입니다.
유한양행은 최근 3년간 레이저티닙(제품명 렉라자)의 개발비 자산화를 통해 무형자산 증가를 이루고 있다. 지난 3년새 무형자산이 566억원에서 1200억원으로 2배 증가했다. 같은 기간 자산화한 개발비는 35배 증가했는데 레이저티닙 개발비의 비중이 가장 컸다.유한양행이 지난해 자산으로 인식한 개발비는 총 1048억원이다. 전년 수치인 717억원과 비교하면 46% 늘었다. 이 중 레이저티닙 임상 3상 비용이 879억원으로 전체의 84%를 차지했다.
◇개발비 자산화 3년새 30억→1048억으로 35배
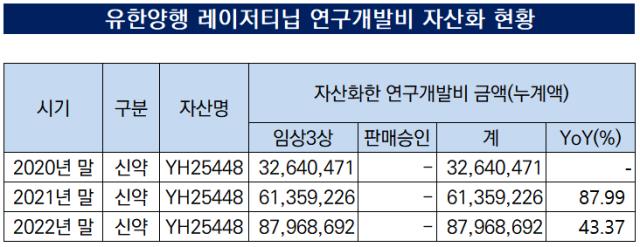
유한양행은 2019년부터 자산화한 개발비 현황을 사업보고서 재무제표 주석에 공시하고 있다. 2019년에는 개량신약 3종으로 시작해 30억원을 자산화했다.
나머지 파이프라인들과 차별화된 '신약'인 레이저티닙의 자산화는 2020년부터 시작됐다. 자산 인식 첫 해에 3상 비용은 326억원으로 단숨에 무형자산 규모를 끌어올렸다. 작년말에는 3상 누적 비용이 879억원으로 늘어나 자산 총계에 보탰다.
비용으로 기록된 전임상, 임상 1상, 2상 단계의 지출까지 합하면 레이저티닙 연구개발비 전액은 훨씬 클 것으로 전망된다.
2018년 금융감독원이 발표한 '제약바이오 R&D 연구개발비 회계처리 관련 감독지침'에 따라 신약은 임상 3상 IND 승인 이후부터 투입된 비용을 무형자산으로 인식할 수 있다. 바이오시밀러는 임상1상, 제네릭은 생동성시험계획 승인, 진단시약은 허가신청 및 외부 임상신청 등 제품 검증을 한 상태부터 자산화 가능하다.
유한양행이 보유한 임상 3상 단계 파이프라인은 레이저티닙 외 모두 개량신약(6종)이다. 고혈압·고지혈 2제(저용량)/3제/4제 복합제와 저용량 탈모치료제다.
판매가 시작된 고혈압·고지혈 3제 복합제와 위염치료제는 자산화한 후 상각을 거치고 있다. 작년 133억원의 상각이 적용됐다. 상각을 고려한 작년말 개량신약군의 자산가치는 168억원이었다.
◇레이저티닙 3상 종료시점은 특정 불가
레이저티닙은 이미 국내에서 판매를 하고 있지만 임상 3상은 계속 진행 중이라 개발비 자산화도 이어지고 있다. 상각은 아직 시작하지 않았다.
레이저티닙은 기존 치료제에 내성이 생긴 비소세포폐암을 치료하는 3세대 표적치료제 신약이다. 8년 전인 2015년 오스코텍과 제노스코로부터 전임상 직전 단계에 기술도입했다. 유한양행이 물질 최적화와 공정 개발, 전임상과 임상을 진행했다.
임상 3상이 완료되기 전에 조기에 조건부 허가를 득했다. 2021년 1월 국내에서 EGFR T790M 돌연변이 양성 '2차 치료제'로 허가받아 80밀리그램 용량으로 출시했다. 올해 3월에는 더 나아가 '1차 치료제'로 적응증을 추가·변경 허가 신청을 했다.
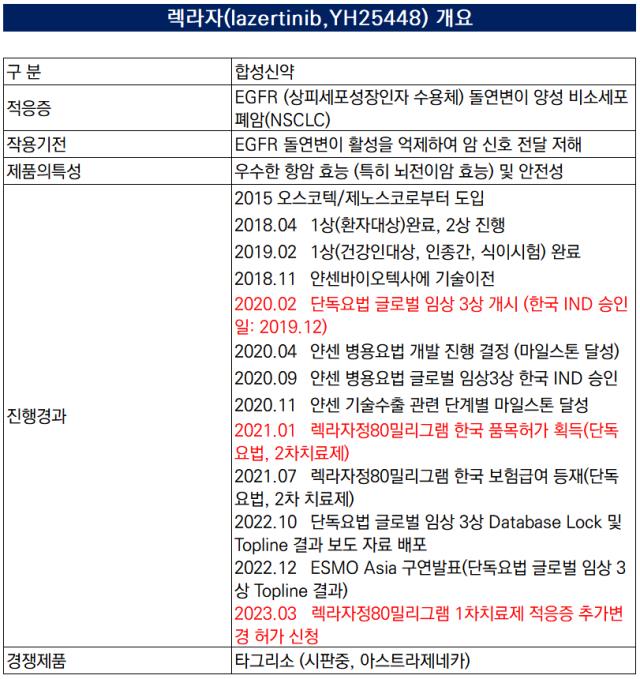
레이저티닙은 임상 3상을 시작한 2020년부터 개발비 자산화를 진행 중이다. 3상 비용은 2020년 326억원→2021년 287억원→2022년 266억원이었다. 매해 3상 비용이 소폭 축소되어 가는 점이 감지된다.
유한양행 관계자는 "일반적으로 임상 시작 초기에 환자모집 등의 이유로 비용 지출이 더 크다"고 설명했다. 또 "3상 종료 시점은 특정할 수 없다"며, "레이저티닙 임상에 참여했던 폐암 환자들이 생존해 있는 동안은 프로젝트를 종료할 수 없기 때문"이라고 말했다. 다만 환자의 모수가 줄어들수록 비용을 계속 자산화할지는 미지수라고도 말했다.
한편 레이저티닙의 글로벌 판권(국내 제외)은 2018년 얀센(Janssen)에 기술이전해 병용 임상 3상을 진행 중이다. 유한양행이 지출하는 비용은 없다.
얀센이 진행하고 있는 레이저티닙과 아미반타맙 병용 임상 3상은 경쟁제품인 타그리소가 실패한 환자 대상이며 최종결과를 연내 발표할 것으로 전망되고 있다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- 수은 공급망 펀드 출자사업 'IMM·한투·코스톤·파라투스' 선정
- 마크 로완 아폴로 회장 "제조업 르네상스 도래, 사모 크레딧 성장 지속"
- [IR Briefing]벡트, 2030년 5000억 매출 목표
- [i-point]'기술 드라이브' 신성이엔지, 올해 특허 취득 11건
- "최고가 거래 싹쓸이, 트로피에셋 자문 역량 '압도적'"
- KCGI대체운용, 투자운용4본부 신설…사세 확장
- 이지스운용, 상장리츠 투자 '그린ON1호' 조성
- 아이온운용, 부동산팀 구성…다각화 나선다
- 메리츠대체운용, 시흥2지구 개발 PF 펀드 '속전속결'
- 삼성SDS 급반등 두각…피어그룹 부담 완화
























