비디아이 "엘리슨, '글루포스파미드' 임상 3상 정상화" 미국 16개 지역·22개 기관 480명 대상, 코로나19로 지연…ILC 중국 2상 이어 FDA 승인 대기
신상윤 기자공개 2021-05-10 15:37:19
이 기사는 2021년 05월 10일 15:34 thebell 에 표출된 기사입니다.
코스닥 상장사 비디아이는 10일 코로나19로 지연됐던 미국 '엘리슨파마슈티컬스(엘리슨)' 췌장암 치료 신약인 '글루포스파미드' 임상 3상이 정상화됐다고 밝혔다.엘리슨이 정기보고회를 통해 알린 이 소식은 글루포스파미드에 대한 임상 완료와 FDA 신약 등록 등으로 늦어도 오는 2023년 판매까지도 기대되는 상황이다.
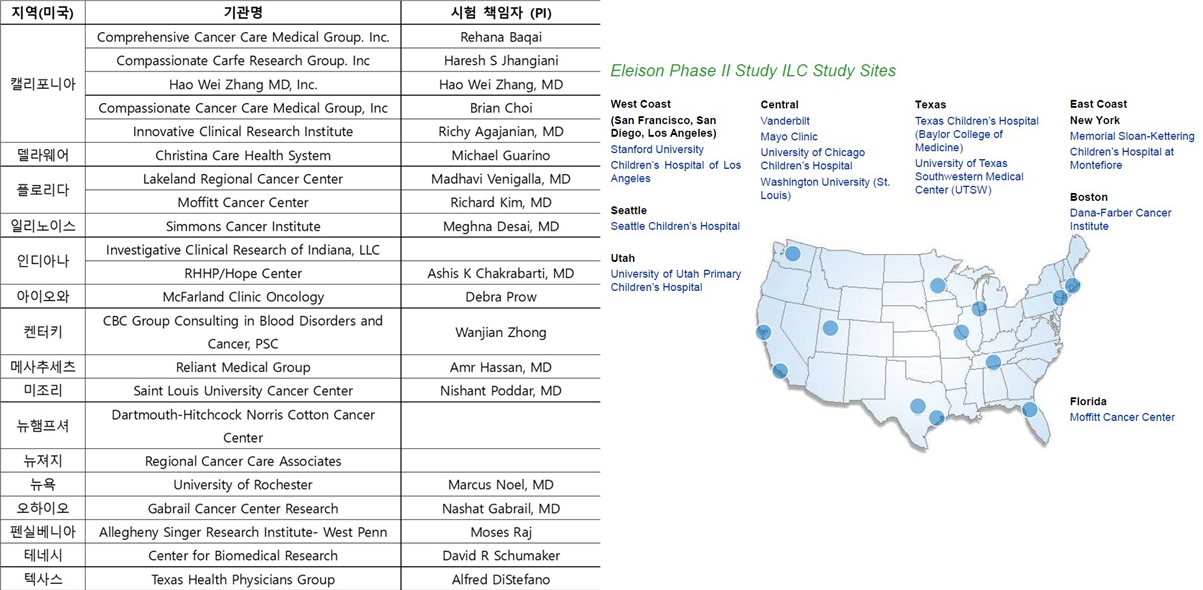
엘리슨은 미국 내 16개 지역의 22개 임상 시험기관에서 480명 환자를 대상으로 글루포스파미드 임상 3상을 진행했다. 다만 최근 코로나19 영향으로 인적 교류가 중단돼 임상이 지연됐다.
비디아이 관계자는 "글루포스파미드 구체적 임상 효능 데이터는 표준 규제 요건에 따라 접근할 수 없지만 안전 데이터는 정기적으로 통보받고 있다"며 "현재까지 새로운 안전 문제는 발견되지 않았고 임상도 순조롭게 진행되고 있음을 보고받았다"고 말했다. 이어 "내년 하반기 아시아와 유럽 등에 신규 등록도 가능해 글루포스파미드 임상에 속도가 붙을 것"이라고 예상했다.
이와 함께 엘리슨은 흡입식 폐암 치료제 'ILC' 임상 2상과 3상 내용을 추가로 보고했다. 지난해 2월 중국에서 임상 2상이 시작한 데 이어 올해 4월에는 미국 FDA에 임상 2상과 3상 시험계획서를 제출해 최종 승인도 기다리는 중이다. 올해 하반기 승인을 받으면 240명 환자를 대상으로 임상 시험을 진행할 계획이다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 인더스트리
-
- 디딤이앤에프, 신규 브랜드 2종 론칭 '매출 확장'
- 대동모빌리티, S-팩토리 자가용 태양광 발전소 준공
- '벼랑 끝 격돌' 대유위니아 vs 홍원식, 전부 걸었다
- [ICTK road to IPO]경쟁자 없는 '차세대 보안칩', 2000억 후반 밸류 '정조준'
- CG인바이츠, 화일약품 지원 축소 11년 동행 '선긋기'
- [K-바이오 클러스터 기행|대전]대전 바이오 구심점, 20년 역사 바이오헬스케어협회
- 코인원, 이용규 CPO 영입…신규 서비스 출시 속도
- [코스닥 코스메틱 리뉴얼]마스크팩 잘나가던 지피클럽, 색조화장 '코디 인수'
- [K-배터리 밸류업 리포트]'오너 경영체제' 원준, 승계작업 '언제쯤'
- [바이오텍 유증·메자닌 승부수]브릿지바이오, 유무상증자에 '대표 지분 블록딜' 왜?
신상윤 기자의 다른 기사 보기
-
- [thebell desk]'부동산 PF' 누가 떠안을 것인가
- [건설리포트]삼성물산 건설부문, 분기 최대 영업이익 달성
- [2024 건설부동산 포럼]"부실 PF 분산·유동성 지원책 필요, 세제 혜택도 해법"
- 디벨로퍼 시티코어, 서소문 개발 사업 본PF 전환 '첫발'
- [디벨로퍼 리포트]일레븐건설, 주춤했던 외형 성장 다시 '기지개'
- [건설리포트]주택 키운 제일건설, '실적·재무' 두토끼 잡았다
- 서희건설, 오너 지배력 강화 '애플이엔씨·자사주' 투트랙
- [건설산업 스몰캡 리포트]우원개발, 부동산 개발업 재시동 '차입 활용' 속도
- 역대급 실적 '엠디엠그룹', 현금성 자산 4000억 웃돈다
- 우원개발, 원가율 부담 속 '재무통' 이사회 합류





















