제테마, 국내 데이터로 중국 2상 건너뛰고 '3상부터' 1조2000억 시장 절대 우위 제품 없어…새 파트너 덕 미국 임상 병행 체력 비축
최은수 기자공개 2024-04-01 08:15:43
[편집자주]
혁신신약을 노리는 기대주, 즉 파이프라인에 대한 가치 평가는 어렵다. 품목허가를 너머 성공적인 상업화에 도달하기까진 임상 평가 지표 외에도 시장 상황, 경쟁사 현황, 인허가 과정이 얽혀 있다. 각사가 내놓는 임상(Clinical) 자체 결과는 물론 비정형화한 데이터를 꼼꼼히 살펴야 하는 이유가 여기에 있다. 국내 주요 제약사와 바이오텍의 주력 파이프라인을 해부해 본다.
이 기사는 2024년 03월 28일 14:57 thebell 에 표출된 기사입니다.
보툴리눔톡신 제제 개발기업 제테마가 국내 임상 데이터를 토대로 중국에서도 2상을 건너뛰고 단번에 3상에 진입했다.유효성과 안전성을 함께 보는 후기임상에서 당초 대비 일정이 지연된 부분을 어느 정도 만회했다. 다만 미국 진출을 위한 드라이브를 거는 중에 500명 해외 임상이 또 추가된 데 대한 부담은 있다.
◇중국 첫 임상 승인 14개월 만 2상 건너뛰고 3상까지
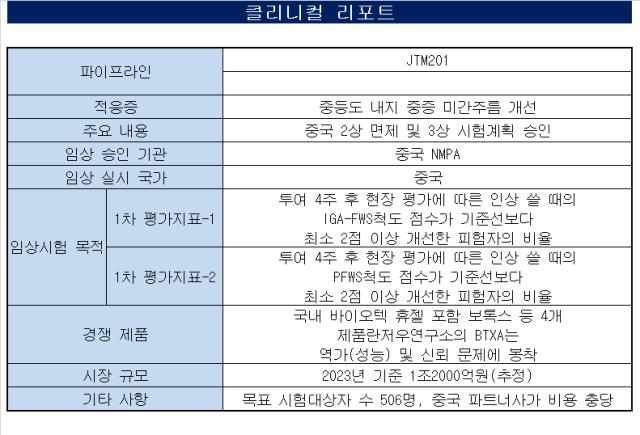
제테마는 최근 중국 국가약품감독관리국(NMPA)으로부터 'JTM201'의 중국 임상 3상을 승인받았다. 작년초 1·2상의 시험계획을 승인받은 지 약 14개월 만이다.
국가전략자산에 해당하는 보툴리눔톡신 균주의 경우 한층 엄격한 출처 및 효능 검증을 해야 해외 반출과 임상이 가능토록 규제가 강화됐다. NMPA는 각 국가에서 별도로 진행한 임상 3상에 준하는 자료를 제출토록 제도를 강화하기도 했다.
제테마의 핵심 파이프라인인 'JMT201 프로그램'은 NMPA 측에서 요구한 국내 임상 3상과 관련한 데이터를 갖고 있던 상황이다. 이에 중국 식약당국에서도 개발 진척 사항에 대해 인정받을 수 있다. 덕분에 중국에선 별도의 추가 자료 없이 2상을 건너뛰게 됐다.
NMPA는 자국 보툴리눔톡신 시장 안정화와 내수제품 드라이브 등을 목적으로 해외 기업에 대한 톡신 인허가 문턱을 지속적으로 높였다. 2022년부턴 인허가를 노리는 해외 기업에 대해 한층 엄격한 규제 요건을 적용했다.
중국 본임상에 진입하려면 재무 체력을 갖추는 것과 각 국가에서 별도로 진행한 임상 3상에 준하는 자료를 NMPA 측에 제출해야 한다. 모국을 포함한 다국가 임상 정보를 규합하는 것도 쉽지 않은데 제테마는 앞서 국내 3상을 마무리했던 점이 승인 호재로 작용했다.
국내서 진행한 임상 3상은 총 306명을 대상으로 유효성과 안전성을 확인했다. 승인 7개월 만인 2022년 11월 전체 환자 모집을 끝냈다. 현재 환자에 대한 후기 투여와 추적관찰 등도 마무리됐다.
중국 임상은 규모가 506명으로 늘었다. 1차 평가지표도 2개로 나눠 데이터를 분석하고 관리한다. 각각 투여 4주 후 현장 평가에 따른 인상 쓸 때의 IGAFWS척도 점수와 PFWS 척도 점수가 기준선 대비 2점 이상 개선한 피험자 비율이다.
◇톡신 국내 3상 환자모집 끝→ 관련 인프라 中 임상 전력투구
제테마가 당장 노리는 국가는 보톡스 1번지인 미국이다. 중국 임상을 통한 성과 창출을 병행하게 된만큼 적기에 투자를 결정하고 세밀한 자금 조달 및 지출 계획을 세워야 한다.
현재 미국 사업은 창업주 김재영 회장이 지휘하고 있다. 작년 말 기준 약 400억원의 현금성자산을 토대로 드라이브를 걸었다. 보툴리눔 톡신 외 필러 판매가 연착륙 단계에 들어섰지만 대규모 중국 임상이 더해질 때의 충격을 버틸 수 있는지는 살펴봐야 한다.
모집 인원이 많지만 새 파트너사인 화동에스테틱스가 임상 비용을 댄다. 현재 중국 시장에 진출한 제품군은 원조격인 애브비(Abbvie)의 보톡스와 또 다른 국내 기업인 휴젤을 포함해 4개다.
다만 이들 제품만으론 1조2000억원에 달하는 톡신 시장을 모두 소화하기란 한계가 있다. 관영기업인 란저우생명연구소의 BTXA는 비록 자국 제품이지만 심각한 성능 및 신뢰 문제에 맞닥뜨렸다.
김재영 회장은 "비록 미국 임상이 가격도 비싸고 처음이지만 분기별 또는 각 마일스톤 달성을 위한 집중적인 비용 집행이 어느 한 지점에 집중되지 않았기 때문에 중국과 동시에 임상을 진행하는 것도 해볼 만하다"고 말했다.
제테마 관계자는 "기존 목표로 하던 시기보다 진출이 소폭 늦어졌지만 파트너십과 긴밀히 소통해 2026년경엔 결과를 받아볼 수 있을 것"이라고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 인더스트리
-
- 현대건설, '힐스테이트 죽림더프라우드' 분양 중
- [Red & Blue]새내기주 한싹, 무상증자 수혜주 부각
- 아이티센, 일본 IT서비스 시장 공략 '잰걸음'
- 소니드로보틱스, 온디바이스 비전 AI ‘브레인봇’ 공개
- (여자)아이들 '우기’, 초동 55만장 돌파 '하프밀리언셀러'
- [ICTK road to IPO]미국 국방산업 타깃, 사업 확장성 '눈길'
- [Red & Blue]'500% 무증' 스튜디오미르, IP 확보 '성장동력 발굴'
- [코스닥 주총 돋보기]피엔티, 이사회서 드러난 '중국 신사업 의지'
- '화웨이 대체자' 삼성전자, 유럽 오픈랜 시장 선점 속도
- [Company Watch]'재매각' 엑스플러스, 증자 추진 '사업기반 리셋'
최은수 기자의 다른 기사 보기
-
- '필러·보톡스' 알에프바이오, 프리IPO 펀딩 착수
- 종근당그룹, 프리미엄 요양원 인수 '100억' 베팅
- 'BNCT로 항암 타깃' 다원메닥스, 코스닥 예심 청구
- [클리니컬 리포트]박셀바이오, '가보지 않은' NK 췌장암 임상 '숨고르기'
- [제일약품의 온코닉테라퓨틱스 첫 '신약']'비상장 바이오벤처' 국산신약, 블록버스터에 도전장
- KDDF, 2기 체제 첫 인사 HLB제약 전복환 대표 영입
- 박셀바이오, 진행성 간세포암 타깃 'Vax-NK' 특허 출원
- 뷰노, '비파괴검사' 강자 이번엔 '안저분석' 혁신기기로
- [바이오텍 상장 재도전기]허리띠 졸라맨 벤처 10년, 건강한 비만약 실마리 찾다
- [클리니컬 리포트]티움바이오, TU2218 항암 적응증 '난치암'으로 확립



















