[루키 바이오텍 in market]이엔셀, 핵심 파이프라인 투트랙 전략 '한 발 더'①EN001 듀센근위축증 이어 샤르코마리투스도 1b상 승인, 2상 후 조건부 품목허가 기대
최은수 기자공개 2023-09-25 10:20:13
[편집자주]
스포츠에서 신인을 뜻하는 루키(Rookie)의 어원은 체스에서 퀸 다음으로 가치 있는 기물인 룩(Rook) 또는 떼까마귀(Rook)다. 전후좌우 자유롭게 이동할 수 있는 점이 신인의 잠재력과 행보와 닮았단 해석, 속임수에 능하고 영악한 떼까마귀같다는 부정 의미도 있다. 기업공개(IPO)를 통해 유동성 공급을 앞둔 '루키 바이오텍'에도 이런 양면성이 내재해 있다. 더벨이 주식시장 입성을 앞둔 이들 기업의 진면목을 살펴본다.
이 기사는 2023년 09월 21일 15:45 thebell 에 표출된 기사입니다.
기업공개(IPO)를 통해 코스닥 입성을 노리는 이엔셀이 핵심 파이프라인 'EN001'의 샤르코마리투스(CMT) 1형 질환 치료제 개발을 위한 임상 1b상을 승인받았다. EN001은 앞서 CMT 외에도 듀센근위축증(DMD) 1b·2상을 진행 중이다. 희귀유전질환을 타깃하는 '임상 투트랙' 전략이 순항하는 모습이다.이엔셀은 임상 진척(Catalyst) 기준으로 보면 IPO 성패를 가늠할 만한 단초인 후기 임상 진입 프로그램이 없다. 그러나 앞서 두 개의 적응증이 모두 난치 질환인 점이 눈길을 끈다. 경우에 따라 동시에 두 개의 프로그램으로 신속승인 문턱을 두드릴 가능성이 제기되는 점은 IPO 국면에서 긍정적인 요인으로 꼽힌다.
◇'삼성가 유전질환' 잘 알려진 CMT… 1A형 타깃 임상 1b상 승인
이엔셀은 20일 식품의약품안전처로부터 EN001의 CMT 임상 1b상에 대한 시험계획을 승인받았다. EN001의 CMT 임상은 2021년 6월 총 12명의 목표시험대상자를 대상으로 안전성과 유효성을 확인하는 1상 프로그램을 승인 받았다. 이번에 1b상(반복투여) 승인이 나면서 후기임상(2상) 진입 전망도 한층 밝아졌다.

EN001이 타깃하는 CMT는 대표적인 난치성 유전 질환이다. 종류가 여러가지인데 PMP-22 등 특정 유전자의 중복으로 손이나 발, 말초신경의 정상적인 발달이 저하되는 게 대부분이다. 흔히 손이 굽고 마비가 오며 국내에선 삼성 일가의 유병 사례가 알려지며 유명세를 탔다. EN001은 여러 CMT 가운데 1A형을 타깃한다.
EN001 CMT 1b상의 세부 설계 내용은 공개되지 않았다. 다만 1상이 안전성 및 내약성, 투약량 확정을 위해 소규모 인원에서 진행되는 점, CMT 치료를 위해선 반복투여가 필요한 점을 고려하면 앞서 진행한 1a상과 설계나 규모는 대동소이할 것으로 보인다.
앞서 1a상에선 총 12명의 환자를 모집했다. 해당 임상 프로그램은 오는 2026년 12월까지로 예정했었다. 더불어 기존 임상 1상의 1차 평가지표는 EN001의 투여 후 용량 제한 독성(DLT) 확인 및 최대 내약 용량(MTD) 용량 수준 결정 등이다. 2차 평가지표는 이상반응 및 활력깅후, 보행및 균형기능 변화, 걷기 검사, 하지 MRI 검사 결과 등으로 채웠었다.
이밖에 장기 안전성 평가(탐색적 유효성)를 위해 약물 용량을 나눠 정맥 투여를 진행했다. 유전검사를 통해 CMT 1A형으로 진단받았으며 만 19세 이상 만 75세 이하의 남녀를 대상으로 삼았다. 이엔셀의 EN001은 핵심 모달리티(치료접근법)은 동종인간탯줄유래 중간엽 줄기세포다. 원천기술 ENCT (ENCell Technology) 방법으로 세포를 분리 배양했다.
◇또 다른 희귀질환 듀센근위축증도 2상 진입… '패스트트랙' 통한 이른 상업화 기대
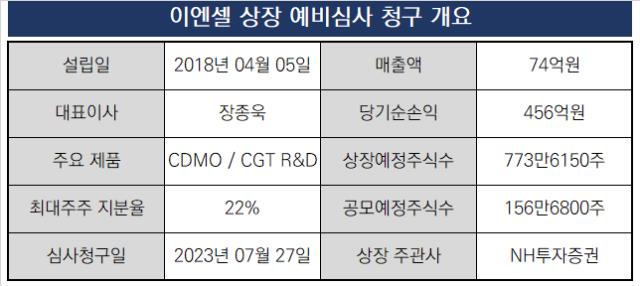
이엔셀은 올해 초 기술성평가 후 코스닥 상장을 위한 예비심사를 청구해 본격적인 IPO를 시작했다. 장종욱 삼성서울병원 교수가 2018년 창업했다. 삼성서울병원이 주도하는 교수 창업(스핀오프) 기업이다.
통상 예심 문턱을 넘으려면 혁신 기술이거나 수 년 내 상업화가 가능한 후기 임상 프로그램을 보유해야 한다. 이엔셀은 EN001로 또 다른 희귀유전질환인 DMD 질환 치료제를 개발 중인데 이 역시 난치성 희귀질환인 점에 초점을 맞추고 있다.
해당 임상은 1b·2상을 수행 중이다. 앞서 CMT와 마찬가지로 DMD 역시 마땅한 근본치료제가 개발되지 않았다. 글로벌 단위로 봐도 사렙타테라퓨틱스의 엘레디비스가 유일하다. 엘리디비스 출시 전엔 근육 쇠약을 늦추는 약물(코르티코스테로이드)이나 운동 치료 등 대체 요법만이 처방돼 왔다.
이에 따라 현재로선 앞서 파이프라인의 후기임상에서 일정 수준의 유효성만 확보하면 가속승인(신속승인) 절차를 통한 조기 상업화의 길이 열릴 가능성이 높다. 해외에서 앞서 출시된 엘레디비스 또한 효능과 안전성 전반에서 의구심이 컸지만 '시급성'을 이유로 승인 문턱을 넘어섰다.
이엔셀 관계자는 "이번 반복투여 임상시험에서는 CMT환자에게 총 2번의 반복 투여를 통해 안전성과 유효성을 재차 확인할 예정이며, 임상 결과에 따라 조건부 품목허가를 비롯한 가속승인을 기대하고 있다"고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- [북미 질주하는 현대차]윤승규 기아 부사장 "IRA 폐지, 아직 장담 어렵다"
- [북미 질주하는 현대차]셀카와 주먹인사로 화답, 현대차 첫 외국인 CEO 무뇨스
- [북미 질주하는 현대차]무뇨스 현대차 사장 "미국 투자, 정책 변화 상관없이 지속"
- 수은 공급망 펀드 출자사업 'IMM·한투·코스톤·파라투스' 선정
- 마크 로완 아폴로 회장 "제조업 르네상스 도래, 사모 크레딧 성장 지속"
- [IR Briefing]벡트, 2030년 5000억 매출 목표
- [i-point]'기술 드라이브' 신성이엔지, 올해 특허 취득 11건
- "최고가 거래 싹쓸이, 트로피에셋 자문 역량 '압도적'"
- KCGI대체운용, 투자운용4본부 신설…사세 확장
- 이지스운용, 상장리츠 투자 '그린ON1호' 조성
최은수 기자의 다른 기사 보기
-
- [Board change]합병 앞둔 한화인더스트리, '비전 C레벨' 이사회 합류
- [캐시플로 모니터]한화오션, 2조 유증에도 아쉬운 현금흐름 '또 차입'
- DB금투, '약식명령'에 저축은행 대주주 적격성 흔들
- [CFO 인사 코드]'변화대신 안정' 미래에셋그룹, 재무라인 교체 '없었다'
- [On the move]'그룹 넥스트' 찾는 삼성물산, '신사업 팔방미인' 공채
- 명륜진사갈비의 '변신을 위한 용기'
- [2024 이사회 평가]'AI 투자회사 변신' SK네트웍스, 힘 보태는 이사회
- [2024 이사회 평가]'사내이사 없는 이사회 고수' 한샘, 참여도만 '우수'
- [조달전략 분석]포스코홀딩스, 급전 융통 창구된 '해외 계열사 지분'
- [Board change]'보험 키맨' 필요했던 롯데손보, 금감원 출신 영입






















