[클리니컬 리포트]펙사벡만 있다? 신라젠, '저분자화합물'로 전략 다각화BAL0891, FDA에 저분자 항암제 1상 IND 변경 신청…'펙사벡' 이후 7년만 본임상
차지현 기자공개 2024-02-05 08:19:19
[편집자주]
혁신신약을 노리는 기대주, 즉 파이프라인에 대한 가치 평가는 어렵다. 품목허가를 너머 성공적인 상업화에 도달하기까진 임상 평가 지표 외에도 시장 상황, 경쟁사 현황, 인허가 과정이 얽혀 있다. 각사가 내놓는 임상(Clinical) 자체 결과는 물론 비정형화한 데이터를 꼼꼼히 살펴야 하는 이유가 여기에 있다. 국내 주요 제약사와 바이오텍의 주력 파이프라인을 해부해 본다.
이 기사는 2024년 02월 01일 16시50분 thebell에 표출된 기사입니다
신라젠이 스위스 제약사로부터 도입한 항암제 후보물질의 자체 임상에 나선다. 회사 정체성과도 다름없던 항암 바이러스가 아닌 '저분자화합물' 기반 신약 임상에 진입한다는 점이 눈길을 끈다. 한 영역에 치우쳤던 포트폴리오를 다각화해 리스크 관리에 만전을 기한다는 목표다.◇BAL0891 1상 IND 변경 신청…적응증·시험자 수 등 확장
신라젠은 1일 미국 식품의약국(FDA)에 항암제 후보물질 'BAL0891' 임상 1상 임상시험계획(IND) 변경을 신청했다고 밝혔다.
BAL0891은 신라젠이 2022년 9월 스위스 로슈에서 분사한 '바실리아'라는 회사로부터 총 계약금 3억3500만달러(약 4370억원), 선급금(업프론트) 200억원을 주고 도입한 물질이다. 모달리티는 저분자화합물로 TTK와 PLK1을 동시에 억제하는 기전이다. 바실리아는 신라젠과 계약을 맺기 전 BAL0891에 대해 전이성고형암 환자를 대상으로 FDA 1상 IND를 허가받았다.
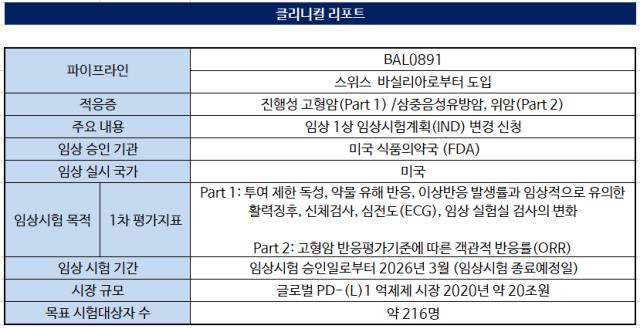
신라젠은 하위 연구를 추가하기 위해 이번 IND 변경을 신청했다. 삼중음성유방암과 위암 환자를 대상으로 용량 확장 임상을 추가한다.
세부적으로 △진행성 고형암 환자를 대상으로 BAL0891 단독 및 카보플라틴 또는 파클리탁셀을 병용 투여하는 Part1 △RP2D(임상 2상 권장용량) 확립 시 삼중음성유방암과 위암 환자를 대상으로 BAL0891 단독 및 파클리탁셀을 병용 투여하는 Part2로 나눠 임상을 진행할 예정이다.
목표 시험 대상자 역시 96명을 추가했다. 이로써 총 216명 환자를 모집할 예정이다. 기존 평가지표였던 안전성과 내약성 탐색에서 나아가 임상 1상 단계서 유효성까지 평가하겠다는 구상이다.
신라젠 관계자는 "이번 임상 변경 신청은 사전에 계획된 것"이라며 "현재 진행 중인 임상에서 특이한 문제점 및 이상사항이 발견되지 않아 계획대로 변경 및 확대를 신청하는 것"이라고 말했다.
◇항암 바이러스 원툴 아니다…저분자로 영역 넓혀 리스크 헤지
BAL0891 임상 진입이 갖는 의미는 크다. 대표 파이프라인 '펙사벡'의 글로벌 임상 좌초 이후 7년 만에 본임상 진입 사례라는 데 더해 항암 바이러스에 치우친 포트폴리오를 다각화한다는 측면에서 주목할 만하다.
항암 바이러스는 신라젠에 있어 정체성과 다름없었다. 항암 바이러스는 세포 안으로 침입해 복제한 뒤 다시 다른 세포로 옮겨가는 바이러스의 특성을 활용해 암세포를 제거하겠단 개념이다. 펙사벡이 여기에 속한다. 재정비를 마친 신라젠 연구진이 자체 발굴한 'SJ600 시리즈' 모달리티 역시 항암 바이러스다.
신라젠은 여전히 항암 바이러스에 대한 강한 기대감을 드러내고 있다. 글로벌 제약사(빅파마)와 병용 임상은 물론 국내 스타트업 루닛 등과 협업하며 펙사백 기사회생 프로젝트를 가동 중이다. 정맥주사 방식인 SJ600 시리즈의 경우 종양에 직접 주사하던 기존 항암 바이러스 치료제의 단점을 개선했다는 점을 내세우고 있다.
다만 시장에선 항암 바이러스에 대한 우려의 시각이 존재한다. 지금까지 FDA 허가를 받은 항암 바이러스 신약은 미국 암젠의 흑색종 치료제 '임리직'이 유일할 정도로 개발이 어려운 분야로 꼽힌다. SJ-600 시리즈도 아직 전임상 단계에 있는 초기 물질이다. 무엇보다 신라젠은 펙사백을 통해 한 물질에 올인하는 전략의 위험성을 몸소 체감했다.
항암 바이러스 파이프라인에 대한 의존도를 낮추면서 펙사벡과 SJ-607의 연구개발 속도 간극을 메꿔줄 물질이 BAL0891다. 특히 여러 해외 바이오 기업이 TTK와 PLK1을 각각 억제하는 항암제를 개발 중이지만 TTK와 PLK1을 동시에 막는 기전은 BAL0891이 세계에서 유일하다. 개발에만 성공하면 계열 내 최초(First-in-Class) 신약이 될 수 있다는 게 신라젠 측 설명이다.
신라젠 관계자는 "유사분열 체크포인트 억제제(MCI) 계열 BAL0891은 TTK와 PLK1을 동시에 저해하는 first-in-class 신약"이라면서 "현재 미국과 한국에서 임상이 순항 중"이라고 했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- 청약증거금 2조 몰린 쎄크, 공모청약 흥행 '28일 상장'
- [영상/Red&Blue]겹경사 대한항공, 아쉬운 주가
- [i-point]모아라이프플러스, 충북대학교와 공동연구 협약 체결
- [i-point]폴라리스오피스, KT클라우드 ‘AI Foundry' 파트너로 참여
- [i-point]고영, 용인시와 지연역계 진로교육 업무협약
- [i-point]DS단석, 1분기 매출·영업이익 동반 성장
- [피스피스스튜디오 IPO]안정적 지배구조, 공모 부담요소 줄였다
- 한국은행, 관세 전쟁에 손발 묶였다…5월에 쏠리는 눈
- [보험사 CSM 점검]현대해상, 가정 변경 충격 속 뚜렷한 신계약 '질적 성과'
- [8대 카드사 지각변동]신한카드, 굳건한 비카드 강자…롯데·BC 성장세 주목
























