제테마, 보툴리눔톡신 국내 데이터로 미국 후기 임상 '직행' 480명 대상 안전성 및 3상 진행, 506명 중국 임상 병행 '눈길'
최은수 기자공개 2024-07-05 08:54:28
[편집자주]
혁신신약을 노리는 기대주, 즉 파이프라인에 대한 가치 평가는 어렵다. 품목허가를 너머 성공적인 상업화에 도달하기까진 임상 평가 지표 외에도 시장 상황, 경쟁사 현황, 인허가 과정이 얽혀 있다. 각사가 내놓는 임상(Clinical) 자체 결과는 물론 비정형화한 데이터를 꼼꼼히 살펴야 하는 이유가 여기에 있다. 국내 주요 제약사와 바이오텍의 주력 파이프라인을 해부해 본다.
이 기사는 2024년 07월 04일 10:04 thebell 에 표출된 기사입니다.
보툴리눔톡신 제제 개발기업 제테마가 국내 안전성 임상 데이터를 토대로 미국에서 얼리 스테이지 단계인 전임상과 임상 1상을 건너뛰고 2상으로 직행한다. 중국에서도 비슷한 시기 3상을 진행하는 걸 포함하면 1000명에 육박하는 대규모 후기 임상을 동시에 가동하는 셈이다.◇하반기부터 美 현지 모집 시작, 이르면 2025년 완료
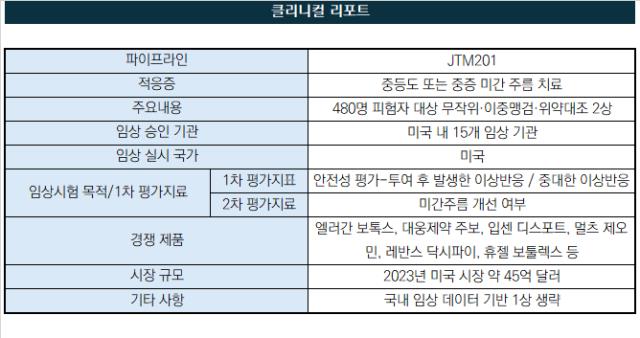
제테마는 올해 하반기부터 자회사 제테마USA를 통해 480명을 대상으로 하는 임상 2상 환자모집을 시작한다. 안전성을 입증하는 1상을 건너뛰고 유효성과 안전성을 함께 보는 후기임상을 먼저 시작하는 점이 눈길을 끈다. 국내 3상을 완료하는 과정에서 안전성을 입증받으며 곧바로 후기임상 길목에 진입할 수 있었다.
당초 미국 사업은 2023년 하반기 초 승인을 목표로 임상 IND 신청을 노렸다. 제반 절차가 늦어지며 IND 제출은 작년 11월 진행됐고 작년말 임상 승인을 받았다. 그러나 승인 과정에서 결과적으로 1상을 건너뛰게 되면서 미국 진출 계획의 지연을 일부 상쇄하게 됐다.
국내 임상 3상을 마무리하고 대규모 유효성 및 안전성 관련 데이터를 확보한 게 주효했다. 올해 2분기 중국에서도 별도의 추가 자료 없이 2상을 건너뛰고 3상을 진입할 수 있었다. 이것도 제테마가 국내서 품목허가 막바지 단계에 들어선 것과 관련이 있다.
임상 2상은 미국 내 15곳의 기관에서 모집 및 투여를 진행한다. 세부적으로 무작위(Random), 이중맹검(Double Blind), 위약대조(Placebo control) 형태로 임상을 설계했다. 이르면 2025년 임상을 완료할 전망이다.
미국은 현재 시장의 80%가량을 '보톡스 원조' 엘러간이 차지하고 있다. 여전히 압도적인 점유율이지만 과거 90% 이상을 점유했던 것을 감안하면 영향력이 다소 축소됐다. 대웅제약이 자체 개발한 보툴리눔 톡신 제제 주보의 시장 점유율을 2023년 12%까지 끌어올리는 약진을 보였다.
미국 기업 레반스의 닥시파이, 국내 기업인 휴젤의 보툴렉스 등도 연이어 품목허가를 따내며 경쟁가도를 형성했다. 일면 과당경쟁의 우려가 보이지만 시장 규모가 약 6조원으로 전 세계 나머지 국가의 총합보다 큰 점이 포인트다. 이론적으로 미국 시장의 약 7%만 차지해도 국내 전체 톡신시장보다 큰 규모의 매출을 확보할 수 있다.
◇글로벌 1000명 임상, 파트너사 지원+국내 품목허가 캐시카우 버팀목
미국 진출을 위한 480명의 임상 드라이브를 거는 중에 500명이 넘는 중국 3상을 함께 소화해야 하는 점은 부담이 된다. 그러나 중국 임상은 새 파트너사인 화동에스테틱스가 임상 비용을 댄다. 개발비용에 대한 부담은 한층 경감된 상태다.
국가전략자산에 해당하는 보툴리눔톡신 균주는 엄격한 출처 및 효능 검증을 해야 해외 반출과 임상이 가능토록 규제가 강화됐다. 특히 중국 인허가기관(NMPA)은 각국에서 별도로 진행한 임상 3상에 준하는 자료를 제출토록 제도를 강화했다. 제테마는 제반 요건을 모두 충족하고 파트너사의 지원까지 받으면서 중국 임상이 순항 중이라고 보고 있다.
제테마의 미국 진출은 창업주인 김재영 제테마 회장이 주도한다. 김 회장은 보툴리눔 톡신개발을 결정하는 순간부터 미국을 겨냥해 목표를 세웠다.
이를 위해 유럽 내 공인된 기관으로부터 오리지널 균주를 도입하면서 업계를 관통한 출처 논란에서 비껴섰고 글로벌 진출을 위한 초석을 다졌다. 임상개시 비용으로 제테마USA에 3백만달러(한화 약 41억원)를 출자한 가운데 추가 지원도 예상된다.
현재 제테마 매출 대부분은 히알루론산(HA) 및 고분자 필러가 차지하고 있다. 이르면 하반기 보툴리눔 톡신의 국내 품목허가가 이뤄지면 글로벌 임상을 지탱할 또 하나의 수익원이 발생하는 데 기대를 걸고 있다.
제테마 관계자는 "미국시장의 빠른 허가진입을 위해 제테마의 우수한 차별점을 기반으로 모든 총력을 기울일 것"이라며 "글로벌 시장의 큰축인 중국을 시작으로 미국에서도 차질없이 임상을 진행할 예정"이라고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 인더스트리
-
- 'HBM 없이도 잘 나간다' 삼성전자, 10조대 영업익 복귀
- [Company Watch]'최대주주 변경' 유니켐, 경영권 분쟁 '일단락'
- [Red & Blue]와이엠텍, 삼성SDI 수주임박 소식에 덩달아 부각
- [광동제약 신사업 전략]효자 '삼다수' 판권 내년 종료, 광동제약 이유있는 확장전략
- [Red & Blue]'중소제약사 인수' 더블유에스아이, 유통 넘어 사업확장
- 엠로, 삼성 편입효과 본격화…글로벌 진출 '가시권'
- [i-point]케이웨더 흡연감지솔루션, SK디앤디 임대주택 적용
- [i-point]폴라리스오피스, 최신 생성형 AI 접목 업데이트 진행
- [i-point]SAMG엔터, 하반기 IP 출격 준비 '수익성 극대화'
- 유유제약 3세, 부친 지분 수증 '세금 낮추고 담보 높이고'
최은수 기자의 다른 기사 보기
-
- 제테마, 보툴리눔톡신 국내 데이터로 미국 후기 임상 '직행'
- 아리바이오, 캐시카우·항노화 확장전략 'HA필러' 탑재
- '1400억 확보' 에이비엘바이오, '4세대 ADC' 거점 미국법인
- [클리니컬 리포트]앱클론, 표준치료 약한 HER2 위암 '새 항암 옵션' 겨냥
- 1시간만에 끝난 HLB FDA 미팅, 'OS 업데이트'에 담긴 의미
- [바이오텍 유증·메자닌 승부수]에이비엘바이오의 버전2 '이중항체 ADC' 기반 대규모 조달
- '젠톡 1년' 마크로젠, 마케팅 광폭 행보 'DTC란 이런 것'
- [클리니컬 리포트]신라젠, 저분자화합물 항암제 도전기 'TNBC·위암 추가'
- 혈액제제 타깃 '파머징' SK플라즈마, 인니법인 힘싣는다
- 프레스티지파마, 다시 돌아가는 '허셉틴 시밀러 인허가 시계'




















