프리시젼바이오의 진단키트 나노체크 차별점 '510(k)' '에이전시' 필요할만큼 높은 승인 난관 뚫고 성과… 감염병 진단 저변 확대 선점
최은수 기자공개 2024-01-30 08:27:42
이 기사는 2024년 01월 25일 07시45분 thebell에 표출된 기사입니다
프리시전바이오가 미국 자회사를 통해 미국 시장에서 정식 의료기기 품목허가(510(k))를 따냈다. 이번 허가는 코로나19 진단제품인 'Nano-Check COVID-19 Antigen Test(이하 나노체크)'의 정식 승인이다. 국내 업체 가운데 긴급사용승인(EUA)이 아닌 정식 절차를 밟아 승인 유일한 사례다.미국은 공중보건비상사태(PHE) 종료 이후 코로나19 키트를 막론하고 의료기기에 대한 EUA 사례를 급속도로 옥죄고 있다. 이 와중에 정공법으로 성과를 내 이목을 끈다. 앞으로 코로나19가 아닌 다른 진단키트를 출시를 놓고도 경쟁사보다 한 발 앞설 기반을 다졌다는 평가다.
◇프리시젼바이오 자회사 나노디텍, 진단 여부 육안 확인 가능 제품 FDA 첫 정식 승인
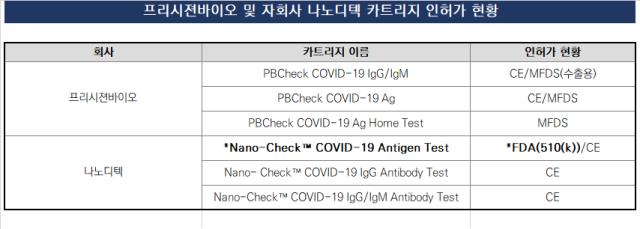
프리시젼바이오의 자회사 나노디텍은 FDA로부터 코로나19 진단제품인 나노체크에 대한 미국 인허가 당국의 '또 한 번'의 승인을 취득했다. 앞서 코로나19 진단 제품에 대한 EUA를 2021년에 받았는데 이번엔 510(k) 가이드라인에 따른 정식승인으로 보인다.
510(k)승인에 대한 사실 여부가 FDA를 통해 정식으로 공시되기까진 약 1주일의 시차가 있다. 다만 프리시젼바이오 측은 보도자료를 통해 "이날 자회사 나노디텍이 510(k)을 취득했다"고 밝히면서 승인 사실을 공식화했다.
프리시젼바이오에 따르면 나노체크는 미국에서 510(k)를 거쳐 정식승인을 받은 스무 번째 진단키트다. 510(k)는 의료기기에 대한 FDA의 포괄적인 인허가 제도를 의미한다. 코로나19 진단키트 역시 의료기기에 해당하는만큼 이 규정에 준해 인허가를 받는다.
다만 다른 의료기기 대비 인허가에 요구하는 가이드라인 허들이 한층 높고 미국 현지 기업이 아닌 곳에 대한 대한 진단키트의 510(k) 승인 사례 역시 상당히 드물다. 나노체크가 전문가용으로 제조된 신속진단 키트 가운데 코로나19 확진 여부를 육안으로 확인할 수 있는 첫 제품인 것도 이와 관련이 있다.
업계 관계자는 "510(k)를 충족하기 위해 준행해야 하는 진단키트와 관련한 가이드라인 허들이 워낙 높다보니 기업이 에이전시를 거치지 않고 자력으로 대응하기도 어렵다는 게 중론"이라며 "이번 나노디텍의 510(k) 획득 자체만으로도 유의미한 성과라는 평가를 내릴 수 있어 보인다"고 설명했다.
◇다른 감염병 진단키트 승인위한 경험치 확보 "RSV·인플루엔자 등 저변 넓힐 것"
프리시젼바이오가 나노디텍을 통해 510(k)를 넘게 된 배경으론 급변하는 인허가 및 규제 환경도 한몫했다. 지금까지 대부분 업체는 오랜 기간이 걸리는 510(k) 대신 PHE에 따라 한시적으로 허용된 EUA를 활용한 빠른 인허가 절차를 거쳤다. EUA는 한시적인 시판 허가를 내준 뒤 일정 기간이 지나면 재검정을 요구하는 제도다.
문제는 미국 FDA에서 PHE가 종료됐다는 이유로 EUA 승인과 재승인 자체를 줄이기 시작한 데 있다. 작년 9월 이후 재승인 사례가 한 건도 나오지 않았다는 점도 이를 뒷받침한다.
이 상황에서 나노디텍이 자력으로 510(k)를 따낸 것은 유리한 정황이다. 특히 승인까지 까다로운 규정을 학습하고 절차를 이해한 점은 나노디텍의 자산과도 같다. 앞으로도 코로나19가 아닌 다른 진단키트에 대한 정식승인을 둔 경쟁에서도 유리한 고지를 차지할 근거로 작용한다.
프리시젼바이오 관계자는 "나노디텍은 감염성 질환에 특화된 진단기업으로 입지를 강화하기 위해 작년부터 호흡기 세포융합 바이러스(RSV) 진단제품 및 코로나19와 인플루엔자 감염 여부를 동시에 검사하는 콤보 제품 등의 미국 임상을 진행하고 있다"며 "임상이 마무리 되는대로 올해 1분기께 FDA 510(k)를 신청할 예정"이라고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- [i-point]배터리솔루션즈 "IPO 계획 변함없다"
- 다나와 "그래픽카드 거래액 증가…신제품 출시 효과"
- 메리츠증권 PBS 진출 사력…NH증권 키맨 영입 '불발'
- VIP운용 조창현 매니저, '올시즌 2호' 4년만에 내놨다
- [2025 주총 행동주의 리포트]머스트의 조용한 '구조 개입'…침묵이 아닌 설계
- 한국증권, 채권형 중심 가판대 재정비
- 알토스벤처스, 크림 구주 인수 검토…1조보다 낮은 밸류
- 한화증권, 해외 라인업 강화 스탠스 '고수'
- [연금시장에 분 RA 바람]금융사도 일임 경쟁 참전…관건은 은행권 확보
- [택스센터를 움직이는 사람들]"고객만족 최우선시, 시나리오별 절세 노하우 제공"
최은수 기자의 다른 기사 보기
-
- [ROE 분석]현대해상, 두자릿수 이익률 이면에 자기자본 소실
- [ROE 분석]삼성화재, 자본감소 최소화하며 효익은 최대로
- [밸류업 성과 평가]10대 그룹 참여도 LG·HD현대 으뜸 한화·GS는 불참
- [밸류업 성과 평가]삼성그룹의 저조한 참여, 계열사 중 삼성화재만
- [밸류업 성과 평가]바이오·헬스 부문 밸류업 참여 다수…엘앤씨바이오 톱
- [밸류업 성과 평가]'FDA 넘은 항암제' 유한양행, 코스피 바이오·헬스 으뜸
- [ROE 분석]두자릿수 이익률 낸 손해보험사 'IFRS17·K-ICS가 기회'
- [ROE 분석]생존 기로 선 중소형 생보사, '이익률' 제고 관건
- [밸류업 성과 평가]건설·부동산 업종 현대건설 뿐, '생존'이 급선무
- [ROE 분석]교보생명, '전략'이 만든 역대 최대 자기자본이익률
























