에이비엘·컴퍼스, 토베시미그 엇갈린 반응 "계획은 이상무" 시장 기대치는 30% ORR, 실제 데이터는 17%…FDA 사전미팅 '착수'
한태희 기자공개 2025-04-03 08:04:59
이 기사는 2025년 04월 02일 15시29분 thebell에 표출된 기사입니다
에이비엘바이오의 'ABL001' 물질을 기술도입한 컴퍼스 테라퓨틱스의 임상 2/3상 톱라인 결과에 시장이 엇갈린 반응을 내놨다. 미국 나스닥 주식시장에서 임상 결과를 발표하자마자 18% 상승해 마감한 컴퍼스 테라퓨틱스와 달리 에이비엘바이오의 주가는 전일 대비 9% 이상 하락했다.시장이 당초 예상했던 객관적 반응률(ORR) 기대치 대비 절반가량 낮은 데이터가 도출된 데 따라 실망 매물들이 나타났다. 그러나 기대보다 낮더라도 초기 유효성을 확인했고 기존 표준치료제 대비 3배 이상의 ORR을 나타냈다는 점에 고무적이라는 평가도 있다.
시장의 관심은 이제 4분기 예정된 무진행생존기간(PFS), 전체생존기간(OS) 등 추가 데이터 발표에 쏠린다. 컴퍼스 테라퓨틱스는 이번 데이터를 기반으로 기존 계획대로 미국 FDA 미팅에 착수하며 신약 가속 승인 심사를 추진하겠다는 입장이다.
◇작년 4월 패스트트랙 지정, 연내 추가 결과 발표
에이비엘바이오의 미국 파트너사 컴퍼스 테라퓨틱스는 현지시각 1일 발표한 담도암 타깃 토베시미그의 임상 2/3상 톱라인 데이터를 기반으로 조만간 미국 FDA와 사전 미팅에 착수한다. 신약 승인을 위해 필요한 자료나 절차에 대해 피드백을 받고 임상 전략을 설정한다는 목표다.
컴퍼스 테라퓨틱스가 담도암 2차 치료제로 개발 중인 토베시미그는 작년 4월 미국 FDA로부터 개발사의 빠른 신약 개발을 지원하는 패스트트랙 지정을 받았다. 연내 추가적인 임상 결과를 발표하고 내년 미국 FDA 가속 신약 승인 신청을 목표로 한다.
담도암은 1차 치료제 대비 2차 치료제의 옵션이 제한적인 암종이다. 1차 치료제로는 PD-(L)1 약물과 화학항암제의 병용요법이 쓰이고 있다. 담도암 2차 치료제의 표준요법인 폴폭스(FOLFOX)의 경우 영국 임상 3상에서 관찰된 ORR은 4.9% 수준이다.
컴퍼스 테라퓨틱스는 임상 2/3상 톱라인 결과 표준치료제 대비 상대적으로 향상된 ORR을 확보했다고 강조했다. 토베시미그와 항암제 파클리탁셀의 병용군의 ORR은 17.1%(19/111)로 특정 바이오마커가 없는 기존 2차 표준치료제 대비 3배 이상 높았다.

하지만 앞서 나온 중간 데이터를 기반으로 시장에서 예측한 ORR 대비 아쉬운 수치라는 평가도 제기되며 시장에선 엇갈린 반응이 나타났다. 국내 권리를 보유한 한독은 앞서 'ASCO GI 2023'에서 담도암 환자 대상 이중항체 신약 토베시미그(HD-B001A)의 국내 임상 2상 결과를 발표했다.
당시 임상은 절제 불가능한 진행성, 전이성 또는 재발성 담도암 환자를 대상으로 토베시미그와 파클리탁셀의 병용요법으로 진행됐다. 앞서 1·2차 전신 항암치료를 받은 환자들을 대상으로 서울대병원을 비롯한 국내 4개 기관에서 진행됐다.
24명의 환자를 대상으로 한 오픈라벨 단일군 임상 유효성 평가 결과 병용투여한 환자의 ORR은 37.5%, 부분관해(PR)는 9건 관찰됐다. 2차 치료로 투여받은 환자 11명 중 7명의 부분관해(PR)가 관찰됐고 63.6%의 높은 ORR을 보였다.
◇특정 바이오마커 제외 전체 시장 타깃, 1차 치료제 연구자주도 임상 개시
컴퍼스 테라퓨틱스는 올해 4분기 무진행생존기간(PFS), 전체생존기간(OS) 결과를 공개한다. 이 결과까지 나와야 신약 허가 가능성 등을 가늠할 수 있다. 당초 업계서는 국내 임상 데이터를 기반으로 미국 임상 톱라인 데이터에서 30% 수준의 ORR을 확보한다면 안정적으로 신약 허가 승인이 가능할 것으로 예상했다.
토베시미그, 파클리탁셀 등 여러 약물을 병용으로 투여함에 따라 발생하는 약물의 안전성 관리 역시 변수로 꼽힌다. 토베시미그의 국내 임상 2상에서는 호중구감소증, 고혈압, 빈혈 등 3등급 이상의 부작용이 보고됐다.
에이비엘바이오는 컴퍼스 테라퓨틱스가 가속 승인 절차를 통해 토베시미그의 신약 허가에 성공하면 치료제 판매에 따른 마일스톤과 로열티를 수령할 수 있다. 담도암 2차 치료제 시장 가운데 특정 바이오마커 환자를 제외한 전체 시장을 타깃으로 한다.
토베시미그의 잠재적 가치는 담도암 1차 치료제 등 기존 파이프라인의 확장 가능성에도 숨어 있다. 담도암 1차 치료제 가능성 평가를 위한 MD앤더슨 암센터의 연구자주도 임상도 개시됐다. 대장암 환자를 대상으로 한 임상 2상 역시 진행 중이다.
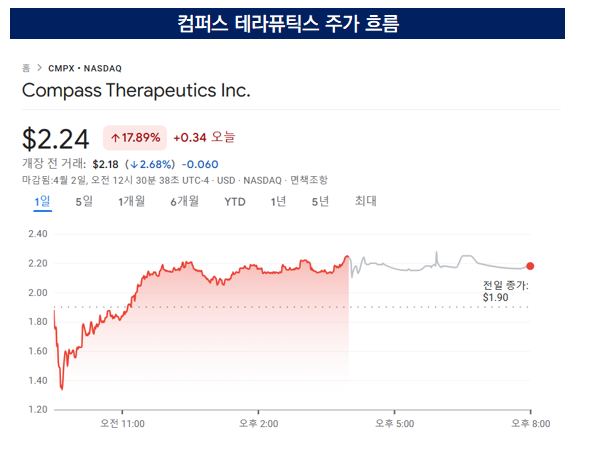
컴퍼스 테라퓨틱스의 주가는 데이터 발표 후 현지 시간 1일 기준 전일 대비 17.9% 상승한 2.24달러로 마감했다. 에이비엘바이오의 주가는 2일 오후 3시 기준 3만3200원으로 전일 대비 9% 이상 하락하면서 상반된 움직임을 보였다.
에이비엘바이오 관계자는 "담도암은 생존율이 낮은 암종으로 2차 치료제 시장도 작지 않고 새로운 약이 생존기간을 늘리면 시장도 함께 커지는 효과가 있다"며 "일부 환자에 적용되는 특정 바이오마커 치료제와 달리 우리 치료제는 전체 환자를 대상으로 한다"고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- 알테오젠 자회사, '개발·유통' 일원화…2인 대표 체제
- [상호관세 후폭풍]포스코·현대제철, 美 중복관세 피했지만…가격전쟁 '본격화'
- [상호관세 후폭풍]핵심산업 리스크 '현실화'...제외품목도 '폭풍전야'
- [상호관세 후폭풍]멕시코 제외, 한숨돌린 자동차 부품사…투자 '예정대로'
- [상호관세 후폭풍]미국산 원유·LNG 수입 확대 '협상 카드'로 주목
- [상호관세 후폭풍]조선업, 미국 제조공백에 '전략적 가치' 부상
- [상호관세 후폭풍]생산량 34% 미국 수출, 타깃 1순위 자동차
- [상호관세 후폭풍]캐즘 장기화 부담이지만…K배터리 현지생산 '가시화'
- [2025 서울모빌리티쇼]무뇨스 현대차 사장 "美 관세에도 가격인상 계획없어"
- [2025 서울모빌리티쇼]HD현대사이트솔루션 대표 "북미 매출목표 유지한다"
한태희 기자의 다른 기사 보기
-
- 에이비엘·컴퍼스, 토베시미그 엇갈린 반응 "계획은 이상무"
- 종근당, R&D 조직 재편 고민…BD임원 신약 수장 등용
- "제조 넘어라" 삼성 바이오 의지, 커지는 삼성물산 존재감
- 에이비엘·컴퍼스, ORR 17% 유의성 충족…가속승인 잰걸음
- '초격차 상장 도전' 알지노믹스, 기술성평가 신청
- 제일파마홀딩스, 장기근속 임원 승진…온코닉 상장 보상
- [thebell interview]이제영 부광약품 대표 "공장확충만 해도 밸류업 직결"
- HK이노엔, '피노바이오 투자' 넥스트 케이캡 'ADC'?
- 부광약품, 1000억 규모 주주배정 유증 '생산능력 확장'
- 롯데바이오, 3년간 7800억 유증…메가플랜트 사활























