[클리니컬 리포트]박셀바이오, 난공불락 간암 면역세포치료제 진전 이룰까임상 2a상 최종 결과 다음달 발표‥조건부허가 통해 품목허가 가속화
홍숙 기자공개 2023-09-01 09:11:56
[편집자주]
혁신신약을 노리는 기대주, 즉 파이프라인에 대한 가치 평가는 어렵다. 품목허가를 너머 성공적인 상업화에 도달하기까진 임상 평가 지표 외에도 시장 상황, 경쟁사 현황, 인허가 과정이 얽혀 있다. 각사가 내놓는 임상(Clinical) 자체 결과는 물론 비정형화한 데이터를 꼼꼼히 살펴야 하는 이유가 여기에 있다. 국내 주요 제약사와 바이오텍의 주력 파이프라인을 해부해 본다.
이 기사는 2023년 08월 30일 14:07 thebell 에 표출된 기사입니다.
박셀바이오가 간암 치료제 개발을 위한 임상 2상 최종 결과 발표를 앞두고 있다. 신약 개발이 어려운 간암 분야에서 후기 임상을 앞두고 있어 상업화까지 가능할 지 시장은 관심있게 지켜보는 분위기다. 박셀바이오는 조건부허가를 통해 품목허가에 속도를 낸다는 계획이다.◇17명 대상 임상 2a상 다음달 마무리...임상 1상 재현성 확보
박셀바이오가 자가유래 자연살해(NK) 세포치료제 파이프라인 'Vax-NK/HCC'의 임상2a상 결과를 다음달 초 발표한다. 해당 임상 결과는 대한종양내과학회 국제학술대회(KSMO 2023)와 미국간학회 국제학술대회(AASLD 2023) 등에서 발표될 예정이다.
박셀바이오는 국내 주요 5개 대학병원에서 진행성 간암을 대상으로 Vax-NK/HCC 임상 2a상을 수행 중이다. 당초 20명을 대상으로 연구를 진행할 계획이었으나 17명으로 임상을 마무리한다는 계획이다. 회사 측은 17명의 데이터로도 충분히 연구를 종료할 만한 임상 데이터를 얻었다고 설명했다.
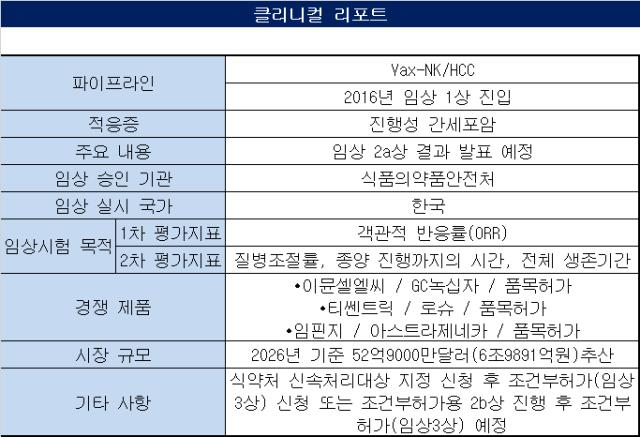
임상 2a상은 암이 있는 국소 부위에 간동맥주입화학요법(HAIC)으로 치료를 받은 진행성 간암 환자를 대상으로 진행됐다. 1차 유효성지표(Primary endpoint)는 객관적 반응률(ORR)이다. 이후 2차지표(Secondary endpoint)인 질병조절률, 종양 진행까지의 시간, 전체 생존기간 등을 통해 일부 유효성을 확인했다.
앞서 진행된 임상 1상은 진행성 간암 환자 11명을 대상으로 진행됐으며 임상 2a상에서도 이와 유사한 결과가 재현됐다. 임상 1상 결과 완전반응(CR) 4명(36.4%), 부분반응(PR) 3명(27.2%), ORR 63.6%, 질병조절율(DCR) 81.8%로 도출됐다. 12명을 대상으로 한 임상 2a상의 중간분석 결과 ORR 66.7%, DCR 100%가 도출됐다.
최근 NK 세포치료제는 단독요법만으로 한계가 있어 병용으로 개발이 진행 중이다. 박셀바이오 역시 이러한 개발 전략에 발맞춰 HAIC와 병용으로 자사의 파이프라인을 간암 치료제로 개발 중이다. 병용요법의 임상적 근거를 강화하기 위해 메타분석을 시행해 기존 전신항암치료와 HAIC와 자사 파이프라인을 병용한 데이터를 간접 비교하는 연구도 진행 중이다.
◇'세포치료제'로 간암 신약 개발 도전...조건부허가 활용 계획
Vax-NK는 암환자의 NK세포를 분리해 박셀바이오의 세포공정 과정을 거친 면역세포치료제 후보물질이다. NK 세포는 우리 몸 속 면역반응을 담당하는 대표적 면역세포로, 다양한 면역반응을 통해 암세포를 직접 공격한다. 뿐만 아니라 다양한 사이토카인을 분비해 또 다른 면역기전을 유발해 암세포를 죽이는 역할을 한다.
박셀바이오는 영양세포주와 낮은 농도의 사이토카인을 활용해 NK 세포의 순도와 증폭률을 높여 Vax-NK를 도출했다. 현재 임상 속도가 가장 빠른 간암 외에도 췌장암과 폐암을 대상으로 한 임상도 진행 중이다.
특히 VAX-NK의 개발 속도가 가장 빠른 간암은 신약 선택지가 많지 않은 암종이다. 간암에선 넥사바(성분명 소라페닙)가 등장한 이후 약 10여년 동안 신약이 등장하지 않았다. 다른 암종과 달리 간암은 단순히 암세포를 죽이는 것 뿐만 아니라 간 기능도 유지해야 하기 때문에 신약개발이 쉽지 않은 상황이다. 실제로 어느 암종보다도 간암 환자는 부작용으로 사망에 이르는 경우가 많다.
넥사바 이후 렌비마(렌바티닙)이 등장했고 이후 면역항암제를 활용한 치료법이 최근 등장하고 있는 상황이다. 최근에 면역항암제인 티쎈트릭(성분명 아테졸리주맙)과 아바스틴(성분명 베바시주맙)을 병용으로 한 치료제가 임상 현장에서 널리 쓰이고 있다. 여기에 면역항암제 임핀지(성분명 더발루맙)와 또 다른 면역항암제 이뮤도(성분명 트레멜리무맙)을 병용으로 하는 치료법도 국내에서 승인을 받았다.
이처럼 최근 간암은 표적항암제에서 면역항암제로 치료 선택지가 넓어지고 있는 상황이다. 이에 박셀바이오 역시 면역세포치료제로 간암 치료제 개발을 가속화 한다는 전략이다. 이를 위해 임상 2a상을 마무리하고 임상 2b상를 조건부허가 품목허가용 임상으로 진입하는 개발 전략도 고려중 이다.
국내에서는 녹십자가 개발한 간암 보조요법 세포치료제로 이뮨셀엘씨가 2007년 품목허가를 받았다. 다만 이뮨셀엘씨는 종양제거술 후 보조요법으로만 처방된다. 이는 암세포를 제거를 직접 타깃으로 하는 박셀바이오의 Vax-NK와는 기전 상의 차이가 있다.
박셀바이오 관계자는 "박셀바이오의 NK치료제는 경쟁사 평균 20일 보다 짧은 14일만에 제조가 가능하다"며 "또한 안정성이 이미 확보돼 고용량으로 투약이 가능한 파이프라인"이라고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
best clicks
최신뉴스 in 전체기사
-
- '메시 네트워크' 메를로랩, 코스닥 출사표
- 에어프로덕츠코리아 예비입찰 흥행 조짐, 대형 PE들 도전장
- SK스페셜티 예비입찰, '한앤코 vs MBK' 붙었다
- [현장 인 스토리]한컴라이프케어, 새 먹거리 '화재진압' 주력
- 폴라리스오피스, '산업단지의 날 기념식'서 이사장상 수상
- [i-point]감성코퍼레이션, 기업가치 제고안 "4분기 중 발표"
- [i-point]ICTK, '서울 유니콘 챌린지' 대상 수상
- 아샘운용 1년만에 수장 또 교체…김대환 대표 사임
- 알펜루트운용 최대주주 교체…김항기 전 대표 엑시트
- 더블유운용, NH증권 루키리그로 랩어카운트 '출격'



















