삼성에피스, 시밀러 FDA 허가 가시권…기대되는 외형성장 스텔라라·솔리리스 시밀러 출격 예정, 마일스톤 수령 기대감
차지현 기자공개 2024-06-12 11:13:01
이 기사는 2024년 06월 11일 09:52 thebell 에 표출된 기사입니다.
삼성바이오에피스의 바이오시밀러가 미국 규제당국의 잇단 허가를 앞뒀다. 자가면역질환 치료제, 희귀질환 치료제 등 바이오시밀러가 곧 미국 시장서 승인을 받을 것으로 점쳐진다. 연구개발 수수료(마일스톤) 유입에 따른 외형 확장 기대감도 감지된다.11일 바이오 업계에 따르면 삼성바이오에피스의 2개 바이오시밀러 제품이 미국 시장 진입 가시권에 들어왔다. 이달 내 미국 식품의약국(FDA) 허가가 점쳐지는 제품은 얀센의 자가면역질환 치료제 스텔라라 바이오시밀러 'SB17'이다. 앞서 4월 유럽 시장에서는 4번째로 품목허가를 획득한 제품이다.
미국 알렉시온의 발작성 야간혈색소뇨증(PNH) 치료제 솔리리스 바이오시밀러 'SB12'도 FDA 승인이 임박했다. 이르면 내달께 허가를 받을 수 있다는 관측이 나온다.
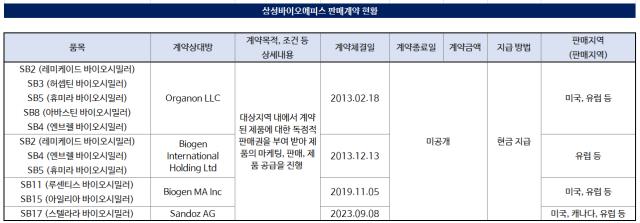
SB12는 작년 5월과 올 1월 각각 유럽과 국내 규제당국의 품목허가를 받았다. 현재 두 국가에서 '에피스클리'라는 이름으로 직판 중이다.
삼성바이오에피스는 최근에도 바이오시밀러 제품의 미국 승인 사례를 만들어냈다. 지난달 20일(현지 시각) FDA로부터 미국 리제네론과 독일 바이엘이 공동 개발한 안과질환 황반변성 치료제 아일리아의 바이오시밀러 '오퓨비즈' 품목허가를 따냈다. 미국 규제당국의 아일리아 바이오시밀러 첫 승인 사례다.
FDA 품목허가를 받는다고 해서 당장 시장에 제품을 출시할 수 있는 건 아니다. 특허 문제 등이 복잡하게 얽힌 데다 원개발사들은 더욱 촘촘한 방어 전략을 세우고 있다. 판매 수익을 기대하기까진 다소 시간이 걸릴 것으로 전망된다.
하지만 제품 허가 마일스톤은 당장 챙길 수 있다. 글로벌 판권을 넘겨준 파트너사로부터 개발 단계 진척에 따라 마일스톤을 수령하는 구조다.
시장에선 이번에 허가 받은 오퓨비즈와 곧 허가를 앞둔 SB17의 FDA 허가 마일스톤 규모를 합하면 2000억원가량이 될 것으로 보고 있다. 오퓨비즈의 판권은 바이오젠이, SB17의 판권은 산도스가 갖고 있다.
이에 따라 삼성바이오에피스의 외형 성장 기대감이 커지는 분위기다. 지난해 창립 12년 만에 '연매출 1조 클럽'에 이름을 올렸다. 국내 제약바이오 업계를 통틀어 최단 기간 내 매출 1조원 달성 기록이다. 기존 상용화 제품이 본궤도에 오르면서 매출을 내는 데 더해 줄줄이 허가까지 앞둔 만큼 매출 성장세가 한층 가팔라질 것이란 분석이다.
삼성바이오에피스의 신약개발 역시 업계의 관심사다. 바이오시밀러에서 신약으로 사업 확장을 선언한 이후 세포·유전자치료제(CGT), 항체-약물 접합체(ADC) 등 여러 모달리티를 저울질 중이다.
지난해 말 국내 바이오벤처 인투셀과 ADC 분야 개발 후보물질 검증을 위한 공동연구 계약을 맺으면서 ADC 영역으로 무게추가 기울고 있다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- [코스닥 상장사 매물 분석]'투믹스 지분 70% 확보' 수성웹툰, 우회상장 가능성은
- [i-point]에스넷시스템, '쌍용레미콘 통합정보시스템' 전환 지원
- [i-point]아이티센 지원 '라잇웨잇', 중기부 '팁스' 최종 선정
- 농금원 "2027년까지 농식품펀드 1조원 추가 조성"
- 머스트운용, 영풍에 주주제안 "자사주 소각하라"
- 코스닥 장수기업의 '뚝심'
- 'MBK 투자처' 메디트, 3Shape와 특허 소송 종결 합의
- [i-point]덕산그룹, 채용 연계형 외국인 유학생 동계 인턴십 모집
- 조병규 행장 연임 불발, 차기 우리은행장 '안갯속'
- [여전사경영분석]한국캐피탈, 업황 악화에도 순이익 경신…빛 본 다각화 효과






















