엔솔바이오 "코로나19 검체채취키트, FDA 긴급 승인" "EnTM, 바이러스 회수율 95% 이상·고온에서도 안정성 확인"
강인효 기자공개 2021-05-03 10:19:48
이 기사는 2021년 05월 03일 10:19 thebell 에 표출된 기사입니다.
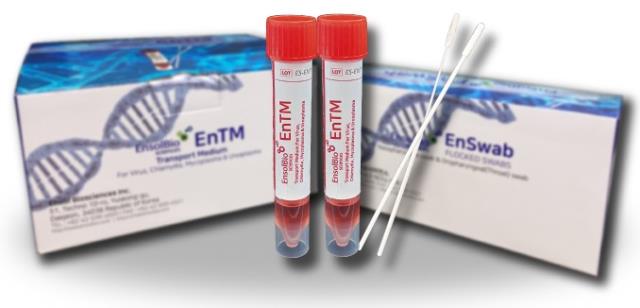
엔솔바이오사이언스(이하 엔솔바이오)는 신종 코로나바이러스 감염증(코로나19) 진단에 필요한 검체 채취 키트 ‘EnTM’이 미국 식품의약국(FDA)의 긴급 사용 승인(EUA)을 획득했다고 3일 밝혔다.엔솔바이오가 개발한 코로나19 검체 채취 키트인 EnTM은 기존 제품의 문제점들을 획기적으로 개선한 제품이라는 게 회사 측 설명이다.
회사 관계자는 “EnTM 성능시험 테스트 결과 통상 요구 기준인 48시간을 넘어 96시간 경과 후에도 바이러스 회수율이 95% 이상으로 보존성이 매우 우수하다”고 말했다.
이어 “안정성 시험 결과 실온 안정성 1년이 확보됐을 뿐만 아니라 40℃에서 9개월(열대 지역 대비), 60℃에서 3개월(극한 조건)에서도 안정성이 확인됐다”고 덧붙였다.
EnTM의 핵심인 배지액(EnTM 내용액)은 2㎖에 불과한 붉은 용액으로 겉보기에는 매우 단순해 보인다. 하지만 20여종의 화학 및 바이오 성분이 적합하게 구성돼 유기적인 기능을 발휘하도록 촘촘히 설계된 제품이다.
EnTM은 작년 10월 의료기기 품질관리 기준인 ‘ISO 13485’ 인증을 받았다. 이어 같은해 12월에는 유럽 품질인증인 ‘CE 마크(Mark)’를 획득했다. 이번에 FDA의 EUA까지 받아 모든 국제 기준을 충족하게 됐다.
엔솔바이오는 EnTM의 국내 공급을 위해 조달청 나라장터에 품목 등록을 완료하고, 지방자치단체를 비롯한 공공기관·군부대 등에 납품을 추진한다. 국내 분자진단 전문기업인 솔젠트와 협력해 해외 동반 진출도 모색 중이다. 미국 진단기기 전문판매회사와는 공급 판매 계약을 협의하고 있으며, 상반기 중 공급 계약이 성사될 것으로 기대하고 있다.
이태오 엔솔바이오 부사장은 “코로나19 바이러스 수송 배지 불량으로 발생하는 진단 오류 문제를 인지해 이를 신약 개발 CMC(제조품질관리) 역량을 바탕으로 수송 배지 불량의 근본 원인을 밝혀낼 수 있었다”며 “향후 미국 FDA 정식 의료기기 등록 절차인 ‘510K’ 등록까지도 완료해 글로벌 시장에서 EnTM이 사용될 수 있도록 하겠다”고 밝혔다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- [코스닥 CB 프리즘]서진시스템, 보통주 전환 물량에 30% 할증 풋옵션 '이례적'
- 에쓰씨엔지니어링 자회사 셀론텍, 태국에 ‘카티졸’ 공급
- 메트라이프생명, 잇단 사외이사 재선임...송영록 대표 체제도 유지될까
- [보험사 IFRS17 조기도입 명암]현대해상, 단순한 상품구조 '부채 감소' 효과는 컸다
- [저축은행 유동성 진단]NH저축, '안전자산' 투자가 이끈 유동성 개선
- [저축은행 유동성 진단]우리금융저축 '영업 확대'로 끌어올린 유동성
- [저축은행 유동성 진단]하나저축, 대출 영업 축소 대신 '예치금 확대'
- [외국계 보험사는 지금]한국시장 엇갈린 시선 '매력 감소 vs 전략 요충지'
- [닻오른 롯데손보 매각]금융지주와 사모펀드…관점별 이상적 인수자는
- [캐피탈사 글로벌 모니터]JB우리캐피탈, 미얀마 영업 제한 건전성 관리 만전




















