[클리니컬 리포트]큐라티스, 백신 연령층 영점 조정으로 임상 '속도전'고령층서 '안전성 데이터'만 확보→ 청소년 대상 2b·3상 연계 가능+개발 기간 단축 판단
최은수 기자공개 2023-09-18 13:01:17
[편집자주]
혁신신약을 노리는 기대주, 즉 파이프라인에 대한 가치 평가는 어렵다. 품목허가를 너머 성공적인 상업화에 도달하기까진 임상 평가 지표 외에도 시장 상황, 경쟁사 현황, 인허가 과정이 얽혀 있다. 각사가 내놓는 임상(Clinical) 자체 결과는 물론 비정형화한 데이터를 꼼꼼히 살펴야 하는 이유가 여기에 있다. 국내 주요 제약사와 바이오텍의 주력 파이프라인을 해부해 본다.
이 기사는 2023년 09월 14일 07:11 thebell 에 표출된 기사입니다.
큐라티스가 결핵백신 QTP101의 임상을 자진 철회한 배경에 이목이 쏠린다. 특히 장년 및 노년을 타깃한 임상에서 유효성 데이터보다 안전성을 확보하는 게 먼저라는 판단을 내린 결과다.프로토콜(수행 지침) 변경은 임상 규정에 따라 주성분 변경(메이저 체인지)과 동일하다. 큰 틀에서 비효율을 막기 위해 기존 임상은 취하하고 안전성 임상(1상) 시험계획승인(IND)을 제출한 것으로 보인다. 요지는 앞서 진행중인 청소년 대상 임상이 2b·3상에 다다라 기존 고령층 2상도 건너뛸 수 있다는 판단이 이같은 새 판짜기 원동력으로 보인다.
◇QTP101 2a상 드롭→ 1상서 '안전성' 입증 주력… 2b·3상 돌입 청소년 백신 연계 목표
13일 큐라티스는 지난 6월 신청한 '장년 및 노년을 위한 QTP101 결핵백신의 국내 제 2a상 임상시험계획(IND)'을 자진 취하한다고 공시했다. QTP101은 결핵 항원에 해당하는 ID93에 면역 증강(Ajuvant) 역할을 하는 큐라티스의 독자 기술인 'GLA-SE'를 접목한 후보물질이다.
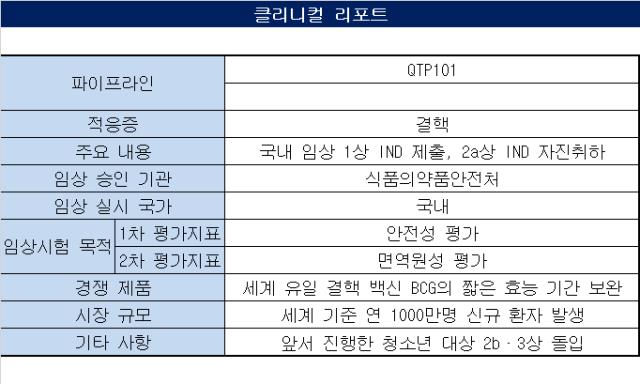
해당 임상은 55세에서 74세의 장·노년을 대상으로 한 결핵백신 후보물질 QTP101의 안전성 및 면역원성을 평가하기 위해 무작위배정과 이중눈가림, 위약 대조 방법으로 진행할 계획이었다.
다만 큐라티스는 해당 임상 2상 대신 장·노년층에 대한 QTP101의 안전성 데이터 확보가 선행돼야 한다 판단하고 2상 자진 취하를 결정했다. 이에 앞서 지난 11일 '성인(55~74세, 장년 및 노년)을 위한 QTP101 결핵백신의 제1상 시험계획(IND)'을 제출하는 것으로 안전성 입증을 위한 제반 절차를 갈음했다.
큐라티스의 의사결정은 기존 진행 중인 청소년 대상 QTP101의 임상이 후기임상 막바지 단계(2b·3상)에 들어선 것과 관련이 있다. 큐라티스의 메인 프로그램이기도 한 청소년 대상 임상은 앞서 고령층 임상보다 모집 인원도 많다. 유효성과 관련한 폭넓은 검증이 가능하다는 뜻이다.
이에 따라 해당 청소년 대상 2b·3상 '유효성' 데이터를 확보하고 나면 이를 장·노년층 임상에도 준용해 프로토콜을 꾸릴 수 있다고 봤다. 요컨대 앞서 청소년 대상 2b·3상에서 안전성이 입증되면 장노년층 임상은 중간 단계인 2상을 건너뛰고 후기 임상 최종 국면에 돌입할 것으로 전망된다.
큐라티스 관계자는 "임상 자진 취하는 결과적으로 장노년층 타깃 백신의 R&D와 상업화 시기를 앞당기기 위한 일보 후퇴 전략"이라고 설명했다.
◇인원은 늘렸지만 총 임상 기간 1개월 단축 "2상 건너뛸 경우 한결 빠른 상업화 기대"
큐라티스가 새롭게 IND를 제출한 임상시험은 1상이다. 다만 모집 인원을 기존 2a상(106명) 대비 120명으로 늘렸고 더불어 임상 기간 또한 기존 임상시험 참여 기관별 임상시험심사위원회(IRB) 승인일로부터 25개월에서 24개월로 줄인 점도 눈길을 끈다.
통상 임상 환자를 소폭 늘리는 것은 임상수행기관이 충분할 경우 전체 수행 기간에 큰 영향을 미치지 않는다. 다만 임상 참여 기간이 한 달 줄었다는 것을 실질적으로 임상 결과를 도출하기까지 기간이 그 만큼 줄어든다는 뜻이다. 큐라티스가 앞서 상업화까지 속도를 높이기 위해 임상 계획 수정에 나섰다는 설명과 부합하는 설계다.
이밖에 대부분의 프로토콜은 대동소이하다. 성인(55~74세)을 대상으로 큐라티스의 결핵 백신 후보 QTP101(ID93+GLA-SE)의 안전성을 평가하고, 면역원성을 탐색하기 위한 무작위배정, 이중눈가림, 위약대조제 1상 임상시험이다. 국내 최대 5개 기관에서 진행된다.
모집 대상은 비시지(BCG)백신 접종력이 있으며, 사람면역결핍바이러스(HIV) 검사 음성인 장년 및 노년(55세 이상 74세 이하)다. 두개의 시험약으로 나뉜 QTP101, 그리고 위약까지 3회 접종 후 안전성을 평가하고 위약 대비 면역원성을 탐색한다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- 신한글로벌액티브리츠, 오피스 비중 '축소'
- [한양증권 매각]SPA 눈앞인데…'대부업 낙인·부동산 매각'에 IB 반발
- 내년 공모채 '준비하는' SK리츠, IB 접점 넓힌다
- [영풍-고려아연 경영권 분쟁]'숨겨진 승자' NH증권, 조단위 브릿지론 '다시 한번'
- 경량 드론 앞세운 에이럭스, 하반기 상장 도전장
- SE인터내셔널, ‘젤라또 피케’ 브랜드로 사업다각화 방점
- 한화에너지 올해 세번째 공모채 출격…2년물 ESG채권
- LS일렉트릭 공모채 시장 복귀…'긍정적' 아웃룩 확보
- 성우하이텍, 400억 P-CBO 찍는다
- [thebell desk]케이뱅크 '상장 트라우마' 해결한 KB증권
최은수 기자의 다른 기사 보기
-
- [비상장사 재무분석]'GS 손자회사' 아크로스, 반기 EBITDA만 350억
- [인벤토리 모니터]HD한국조선해양, '미착품'서도 슈퍼사이클 엿보인다
- [유동성 풍향계]넷마블, '2조' 넘었던 차입금 관리 돌입
- [인벤토리 모니터]한화오션, 적자탈출 트리거 '고점' 다다른 재고자산
- 지식재산(IP)의 아찔한 유혹
- [유동성 풍향계]컴투스, 연이은 IP 활용에도 미미했던 '신작 효과'
- [삼성바이오로직스 vs 셀트리온]배당 예고한 삼성바이오, 자사주 품는 셀트리온
- [On the move]'C2C 거래액 1위' 중고나라 새 CFO 영입 추진
- [Peer Match Up]셀트리온, 이사회 복귀한 서정진 '여전한 영향력'
- [Peer Match Up/삼성바이오로직스 vs 셀트리온]시총 68조 vs 45조…세계 무대에선 여전히 도전자





















