[클리니컬 리포트]프레스티지파마, 'PBP1510' 공략법 '신규 바이오마커'약 없는 '췌장암' 타깃, 자체 발굴 바이오마커 'PAUF'…진단키트도 개발
차지현 기자공개 2023-09-19 11:00:58
[편집자주]
혁신신약을 노리는 기대주, 즉 파이프라인에 대한 가치 평가는 어렵다. 품목허가를 너머 성공적인 상업화에 도달하기까진 임상 평가 지표 외에도 시장 상황, 경쟁사 현황, 인허가 과정이 얽혀 있다. 각사가 내놓는 임상(Clinical) 자체 결과는 물론 비정형화한 데이터를 꼼꼼히 살펴야 하는 이유가 여기에 있다. 국내 주요 제약사와 바이오텍의 주력 파이프라인을 해부해 본다.
이 기사는 2023년 09월 15일 16:00 thebell 에 표출된 기사입니다.
프레스티지바이오파마가 췌장암 항체 신약 임상의 저변을 넓히고 있다. 다섯 번째 국가의 임상승인을 따냈다. 췌장암 영역은 마땅한 치료제가 없다. 새로운 생체표지자(바이오마커) 기반 계열 내 최초(First in Class) 신약으로 경쟁 우위를 점한다는 전략이다.아직 상용화가 안 된 췌장암 조기 진단키트 개발에도 힘을 쏟는다. 최근 미국 행정부 암 정복 프로젝트에 합류하기도 했다. '췌장암 진단-치료' 원스톱 솔루션을 구축한다.
◇PBP1510 싱가포트 1/2a상 승인, 5개국 임상 동시 진행
프레스티지바이오파마는 최근 췌장암 치료제 후보물질 'PBP1510'이 싱가포르 보건과학청(HSA)으로부터 임상 1/2a상 임상시험계획(IND)을 승인받았다고 밝혔다. 미국을 포함해 스페인, 프랑스, 호주에 이은 다섯 번째 국가의 임상 승인이다.
PBP1510 임상 1/2a상은 이미 스페인에서 환자 투약이 시작됐다. 미국에선 미국 식품의약국(FDA) IND 승인 후 하버드 의과대학 부속 매사추세츠종합병원에서 생명윤리위원회(IRB) 심의를 통과해 본격적인 투약 절차를 밟고 있다.
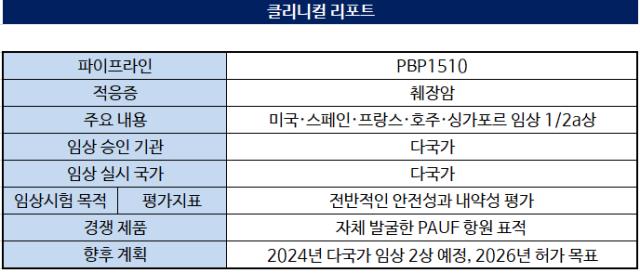
5개 국가를 통틀어 임상 1상에서 30명, 2a상에서 50명을 모집한다. 임상 1상에선 PBP1510의 단일요법 및 기존 췌장암 치료제 '젬시타빈'과 병행요법을 통해 약물의 안전성과 내약성을 확인한다. 이후 임상 2a상에서 약물의 효능을 평가하게 된다.
싱가포르 임상의 경우 싱가포르 국립암센터(NCCS)에서 진행한다. 해당 암센터 종양학 분야 수석 컨설턴트 의사이자 용루린 의과대학 임상 교수인 데이비드 테이 박사가 임상을 총괄을 맡았다. 싱가포르가 의료관광 국가로 떠오르고 있는 데다 정부가 적극적인 지원을 하고 있어 빠르고 정교한 임상이 진행될 것이란 설명이다.
◇신규 바이오마커 'PAUF' 표적, 계열 내 최초 전략
PBP1510은 프레스티지바이오파마가 발굴한 바이오마커 'PAUF'를 표적하는 항체 신약이다. PAUF는 췌장암 환자 80% 이상에서 과발현하는 단백질이다. 앞서 프레스티지바이오파마 혁신신약연구원(IDC)이 PAUF가 체내 면역체계를 교란하고 췌장암 진행·전이를 촉진한다는 사실을 규명했다. PAUF 역할을 원천 차단해 췌장암을 치료하는 게 PBP1510이다.
2020년 유럽 의약품청(EMA), FDA, 국내 식품의약품안전처의 희귀의약품으로 지정됐다. 희귀의약품으로 지정되면 신속한 허가 및 세금 감면 등 혜택을 받을 수 있다. 또 한국·미국·호주 등 세계 11개 국가에서 특허를 취득했다. 유럽·중국 등에서도 특허 심사 절차를 밟는 중이다. 여기에 올 초 FDA 패스트트랙 대상 품목으로도 선정됐다.
췌장암은 미충족 의료 수요가 높은 영역이다. 2019년 기준 5년 생존율이 13.9%가량으로 주요 암종 중에서도 가장 생존율이 낮다. 췌장이 워낙 몸속 깊은 곳에 있어 검진에서 잘 발견되지 않고 완치를 위한 유일한 치료법도 '수술적 절제'뿐이다.
반면 환자 수는 증가하고 있다. 2019년 국가암등록통계 자료에 따르면 췌장암 발생률은 전체 암 가운데 8위를 차지했다.
PBP1510가 표적하는 PAUF 양성 췌장암 환자는 전체 췌장암 환자 46만명의 80%인 37만명. PAUF를 표적해 췌장암 치료제를 개발하고 있는 곳은 프레스티지바이오파마가 유일하다. 개발에 성공하면 계열 내 최초 지위를 확보할 수 있다는 얘기다. 특히 희귀의약품과 패스트트랙 제품으로 지정된 만큼 상용화 시기를 앞당길 수 있다고 보고 있다.
◇'난공불락' 췌장암, 진단·치료 생태계 구축
췌장암 치료제 개발과 함께 진단키트 개발에 나선 점도 눈길을 끈다. 췌장암 조기 진단키트 역시 치료제와 마찬가지로 공식적으로 상용화한 제품이 없는 상태다. 프레스티지바이오파마는 PAUF를 검출하는 진단키트를 개발하고 있다. IDC 연구 결과 자체 개발 췌장암 조기 진단키트의 민감도(양성 진단 비율)가 86.3%로 나타났다.
올 초 국내 특허 가출원을 마쳤다. 제품 상용화에 앞서 특허 기술에 대한 우선권(출원일)을 빠르게 확보하기 위함이다. 내년 상반기 미국과 국내 시장에서 진단키트 제품 상용화를 목표로 인비트로 임상을 준비하고 있다. 인비트로 임상은 사람 대상이 아닌 혈중 PAUF 수치를 확인하는 것으로, 임상 속도가 길지 않다는 게 프레스티지바이오파마 측의 입장이다.
이로써 췌장암 진단부터 치료까지 원스톱 솔루션을 구축한다는 구상이다. 진단키트로 췌장암을 조기진단하면서 신약으로 췌장암 환자를 치료하는 전략이다. '난공불락'으로 꼽히는 췌장암 분야에서 경쟁 우위를 선점, 입지를 넓힐 계획이다.
지난 7월엔 미국 조 바이든 행정부가 추진하는 암 정복 프로젝트 '캔서문샷' 프로젝트에도 합류했다. 오바마 전 미국 대통령이 재임 시절 암 예방·조기 발견·치료제 개발을 위해 국가적인 지원을 하겠다고 밝힌 프로젝트다. 이후 바이든 대통령이 구체화하며 추진하고 있다. PAUF 기반 췌장암 치료 생태계 구축 전략이 선정에 큰 영향을 미쳤다는 후문이다.
프레스티지바이오파마 관계자는 "PBP1510 임상이 순조롭게 본궤도에 진입함에 따라 췌장암 치료 생태계를 구축하려는 행보도 잰걸음을 걷고 있다"며 "마땅한 치료제가 없는 췌장암 영역에서 PBP1510이 세계 최초로 췌장암 정복을 실현하는 새로운 게임체인저가 되도록 임상 진행에 속도를 낼 것"이라고말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
best clicks
최신뉴스 in 전체기사
-
- "최고가 거래 싹쓸이, 트로피에셋 자문 역량 '압도적'"
- KCGI대체운용, 투자운용4본부 신설…사세 확장
- 이지스운용, 상장리츠 투자 '그린ON1호' 조성
- 아이온운용, 부동산팀 구성…다각화 나선다
- 메리츠대체운용, 시흥2지구 개발 PF 펀드 '속전속결'
- 삼성SDS 급반등 두각…피어그룹 부담 완화
- MNC솔루션 고속성장, 'K-방산' 피어그룹 압도
- [DB금투 밸류업 점검]"PIB로 '투자 플랫폼' 기업 도약한다"
- 한컴이노스트림, '도장 인식 시스템' 특허 취득
- [클라우드 키플레이어 MSP 점검] '신생' 안랩클라우드메이트, 최우선 과제 '포트폴리오 강화'
























