[클리니컬 리포트]셀트리온, 첫 당뇨 파이프라인 개발 '복합제' 9부 능선국내외 582명 모집 대규모 임상, 급여 확대 및 해외 진출로 승부수
최은수 기자공개 2024-02-22 08:21:33
[편집자주]
혁신신약을 노리는 기대주, 즉 파이프라인에 대한 가치 평가는 어렵다. 품목허가를 너머 성공적인 상업화에 도달하기까진 임상 평가 지표 외에도 시장 상황, 경쟁사 현황, 인허가 과정이 얽혀 있다. 각사가 내놓는 임상(Clinical) 자체 결과는 물론 비정형화한 데이터를 꼼꼼히 살펴야 하는 이유가 여기에 있다. 국내 주요 제약사와 바이오텍의 주력 파이프라인을 해부해 본다.
이 기사는 2024년 02월 20일 14시42분 thebell에 표출된 기사입니다
셀트리온이 당뇨 복합제 개발 경쟁에 참전했다. 바이오시밀러를 선도하며 안정적인 수익원을 만든 셀트리온이 바이오 혁신신약과 케미컬(합성) 의약품 연구개발(R&D)로도 사업 저변을 넓히고 있다.당뇨병 치료제 가운데 특정 약물을 포함한 복합제가 새롭게 출시되고 보험 급여까지 결정되자 전격적으로 개발에 뛰어든 것으로 보인다.
◇582명 규모 MRCT 착수, 셀트리온그룹 첫 당뇨 복합제 라인업 전망
셀트리온은 19일 식품의약품안전처로부터 'CT-L03'에 대한 다국가 3상 임상시험계획을 승인받았다. 메트포르민과 엠파글리플로진 병용요법으로 혈당조절이 불충분한 제2형 당뇨병 환자를 대상으로 피오글리타존(Pioglitazone) 추가 병용투여 시 유효성 및 안전성을 평가하기 위한 임상시험이다.
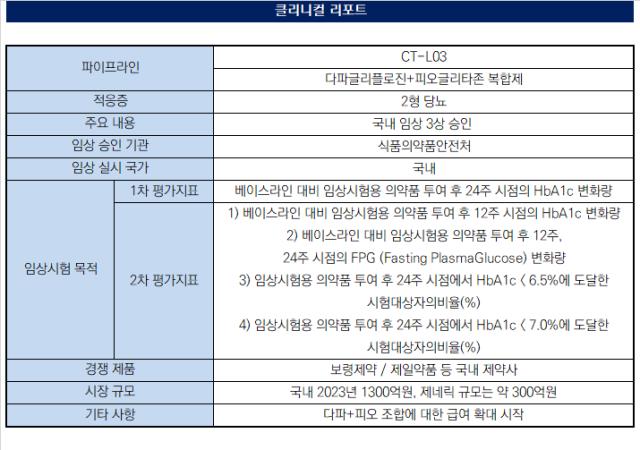
해당 임상은 1차 평가지표를 베이스라인 대비 임상시험용 의약품 투여 후 24주 시점의 당화혈색소(HbA1c) 수치로 설계했다. 2차 평가지표는 12주 지점의 HbA1c와 투여후 12주와 24주 각각에 대한 공복 혈당(fasting plasmaglucose) 변화량이다.
총 582명의 환자를 모집하는 다국가 임상(Multi Region Clinical Trial)으로 진행한다. 이 가운데 국내 모집 예상 환자는 382명에 달한다. 대규모 임상인만큼 국내서만 35곳의 기관을 선정했다. 세부적인 임상형태는 평행·무작위·이중맹검이다.
셀트리온그룹 차원에서 보면 당뇨 케미컬 라인업에 도전하는 건 이번이 처음이다. 'CT-L03'의 세부 정보는 외부 공개가 제한된 모습이다. 다만 앞서 임상 설계와 그룹 내 주목할 만한 당뇨병 치료 후보물질 개발 이력이나 자산 내역이 확인되지 않는 점 등을 고려하면 복합제로 개발될 가능성이 크다.
엠파글리플로진은 자디앙으로 잘 알려진 SGLT-2 억제제 계열 당뇨병 치료제의 주성분이다. 메트포르민은 다케다(Takeda)가 개발한 티아졸리딘디온(TZD) 계열 당뇨병 치료제 '액토스'의 주성분이다. 마침 셀트리온이 2020년 다케다의 아시아·태평양 프라이머리케어(APAC) 중 전문의약품 사업권을 사들인만큼 이를 개발 국면에서 활용할 것으로 전망된다.
셀트리온 관계자는 "개발 중인 파이프라인에 대한 세부 내용은 회사 주요 전략자산에 해당하는 부분이라 별도의 확인이나 언급이 어렵다"고 했다.
◇연이어 개화하는 특정 제제 복합 시장… 내년 임상 종료 목표 시장 지위 확보 분투
셀트리온의 이번 행보는 케미컬 중심의 만성질환 의약품 사업을 확장하겠다는 그룹의 의지로 보인다. 회사 차원에서 꾸준히 글로벌 케미컬 의약품 사업 분야에서 성과 창출에 주력해 왔다. 작년 9월 알로글립틴메트서방정을 허가받은 것을 시작으로 다양한 케미컬 복합제 개발에 뛰어든 상태다.
셀트리온 이번 임상으로 국내외 동시 인허가를 노리는 상업화 타임라인을 꾸렸다. 이 가운데 국내 시장에 먼저 훈풍이 불어온 점은 눈여겨볼 지점이다.
작년부터 다파글리플로진과 피오글리타존에 대한 연이은 품목허가와 급여성과가 나오고 있다. 작년 9월 보령이 처음으로 다파글리플로진과 피오글리타존을 합친 개량신약 '트로버디'를 허가받은 것을 시작으로 작년 12월에는 유영제약, 보령이 출시한 라인업과 동일한 용량(피오다정 10/15mg)을 연이어 허가 받으며 본격적인 경쟁이 시작됐다.
올해엔 제일약품의 '듀글로우정' 역시 동일한 용량(10/30mg)에 대한 품목허가를 따냈다. 기존에 없던 시장이 급속도로 확대되는 국면인만큼 셀트리온이 이 대열에 빠르게 합류하는 전략으로 시장 확보에 나설 것으로 보인다. 무엇보다 500명이 넘는 대규모 임상 종료 시점을 내년 10월로 전망한 것도 의미가 있다는 평가다.
업계 관계자는 "셀트리온은 바이오의약품 사업부문에 이어 합성의약품에서 당뇨병치료제도 영역을 넓히고 있는데 "기존 다케다로부터 확보한 판권과 치료제 라인업을 활용하면서 복합제로 차별화를 모색하는 모습으로 보인다"고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- '아보하' 시장이 그립다?
- 상장 문턱서 좌절한 원유니버스, 넥써쓰가 일으키나
- [아이티켐 IPO]활발한 조달, RCPS·유상증자 당시 밸류 살펴보니
- [판 바뀐 종투사 제도]위험 익스포져 확대 전망, 리스크 파트 설득 '관건'
- [판 바뀐 종투사 제도]PBS 대상 확대…실효성은
- [판 바뀐 종투사 제도]IMA 부동산운용 10% 제한, 발행어음 통합 한도 설정
- 크로스로드파트너스, 에이엘티 투자 1년 만에 회수 '시동'
- 'DIP 카드' 김병주 MBK 회장, 직접 출연 아닌 보증 택했다
- 중부CC 매각 속도전, 홀당 가격 100억 가능 관측
- '고려아연 우군' 베인캐피탈, 브릿지론→인수금융 대환 나선다
최은수 기자의 다른 기사 보기
-
- [ROE 분석]교보생명, '전략'이 만든 역대 최대 자기자본이익률
- [ROE 분석]한화생명, 빅3 중 가장 낮은 이익률 상승세
- [ROE 분석]이익률 상승은 '착시' 생보 빅3도 자본감소 못 버텼다
- [ROE 분석]삼성생명, '업계 맏형답지 않던 이익률' 관리 시작
- [CFO Change]고정석 SK가스 신재생에너지실장, 케미칼 재무총괄로
- [2025 대한민국 사외이사 인식 조사]전문성 기업경영·재무 집중… 한층 두터운 BSM 필요
- [2025 대한민국 사외이사 인식 조사]후보는 누가 '천거'할까 사추위·경영진 막강한 입김
- [ROE 분석]농협금융, 반등했지만 '여전히 은행계지주 바닥권'
- [이슈 & 보드]롯데지주, 바이오로직스 또 베팅 '관세폭풍 두렵잖다'
- [Board Change]'전무 승진' 김성완 애경케미칼 CFO, 사내이사 연임























