[클리니컬 리포트]코오롱생명과학, '통증치료제' 1·2a상 완료…과제는 '유효성'KLS-2031 미국 임상 CSR 수령, 2차 지표 미충족 '후기 임상'서 주력
김형석 기자공개 2024-07-01 09:22:36
[편집자주]
혁신신약을 노리는 기대주, 즉 파이프라인에 대한 가치 평가는 어렵다. 품목허가를 너머 성공적인 상업화에 도달하기까진 임상 평가 지표 외에도 시장 상황, 경쟁사 현황, 인허가 과정이 얽혀 있다. 각사가 내놓는 임상(Clinical) 자체 결과는 물론 비정형화한 데이터를 꼼꼼히 살펴야 하는 이유가 여기에 있다. 국내 주요 제약사와 바이오텍의 주력 파이프라인을 해부해 본다.
이 기사는 2024년 06월 28일 15:52 thebell 에 표출된 기사입니다.
인보사 사태로 내홍을 겪은 코오롱생명과학이 통증치료제 임상을 완료했다. 스테로이드 약물 외 대체약품이 없는 통증 분야의 미충족의료수요에 맞춰 약물을 개발할 계획이다.◇임상 1·2a상 CSR 수령…안정성 입증 결과 도출
코오롱생명과학은 최근 공시에서 신경병증성 통증 유전자 치료제 'KLS-2031'의 미국 임상 1·2a상에 대한 최종보고서(CSR)를 수령했다고 밝혔다.
KLS-2031은 뇌로 가는 통증 신호를 차단하고 뇌 주변 면역 환경을 개선하는 통증치료제다. 재조합 아데노부속바이러스(rAAV)와 치료 유전자 3종을 도입해 뇌로 가는 통증 신호를 차단하고 주변 면역 환경 개선을 목적으로 개발됐다.
코오롱생명과학은 2019년 미국 식품의약국(FDA)의 승인을 받아 2020년 4월 16일부터 작년 10월 5일까지 2년 6개월간 KLS-2031의 임상 1·2a상을 진행했다.
코오롱생명과학은 18명을 대상으로 진행한 이번 시험에서 치료 후 발생 이상반응(TEAEs), 중대한 이상반응(SAE), 약물 관련 이상반응(drug-related TEAEs) 및 조기 중단으로 이어지는 이상반응 등 주요 이상반응을 평가했다.
대상자들은 KLS-2031의 저용량, 중용량, 고용량으로 구분된 세 종류의 코호트와 위약 대조군으로 무작위 배정됐으며, 표적 후근 신경절(DRG) 주변 영역에 경추간공 경막 외 주사가 단회 투여됐다.
104주 차까지 결과에서 이상 반응이 관찰된 사례는 다수 있었다. 다만 대다수의 증상은 약물과의 인과 관계가 '가능성 적은'(unlikely) 것으로 판정받았다.
SAE 반응이 나온 1명의 환자는 양성 폐 신생물(Benign lung neoplasm) 즉 종양이 발견됐지만 증상발현 후 83일째에 회복된 것으로 보고 됐다. TEAEs를 경험한 대상은 총 15명이었다. 저용량 2명, 중용량 4명, 고용량 4명, 위약군 5명 등이다. 이중 약물과 관련된 치료 후 발생 이상반응(drug-related TEAEs)은 총 2명으로 보고됐다.
1명은 고용량군 1명의 대상자에서 알라닌 아미노트랜스퍼라제(alanine aminotransferase, ALT) 상승이 관찰됐다. 이후 증상발현 29일째 회복됐다. 나머지 위약군 1명은 두통과 다한증을 경험했지만 25일째 회복됐다.
◇유효성 입증 실패…후기 임상 핵심 평가 대상으로
하지만 2차 지표였던 유효성은 유의미한 결과를 확보하지 못했다. 투약 52주차에 이중 눈가림과 병용약물 제한을 해제하면서 도출한 유효성 데이터의 신뢰성을 담보하지 못한 탓이다.
코오롱생명과학 역시 "CSR의 유효성 데이터는 보조적인 의미로만 활용가능하다"고 설명했다.
이는 지난해 발표한 중간결과와도 유사하다. 코오롱생명과학은 당시 유의성을 확보하지 못했던 이유로 코로나19 등으로 인한 환자 이탈을 꼽았다.
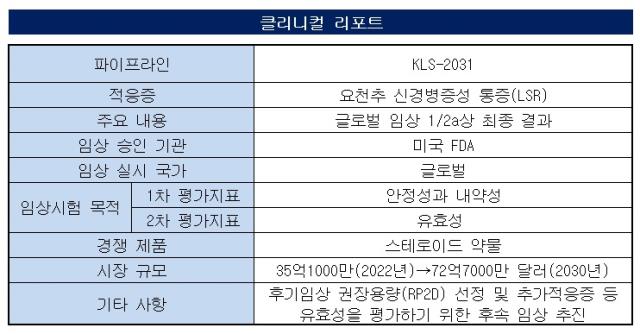
이 때문에 유효성 입증은 향후 진행된 후기 임상에서 핵심이 될 것으로 보인다. 코오롱생명과학 역시 후기 임상에서 권장용량(RP2D) 선정과 추가적응증 등 유효성 평가에 집중하겠다는 입장이다.
코오롱생명과학 관계자는 "별도의 KLS-2031을 투약받은 환자를 대상으로 5년차까지의 장기 안전성 및 내약성 데이터 확보를 위한 장기추적시험을 진행중에 있다"며 "후기 임상에서 RP2D 선정을 비롯해 적응증에 대한 유효성 증명에 집중할 계획"이라고 말했다.
◇미충족 의료 수요에 LSR 시장 규모 연평균 9.5% 성장 '기대감'
신경근병증(LSR)은 아직 완치할 수 있는 치료제가 없다. 통증을 완화하기 위한 스테로이드와 일부 수술요법으로만 치료가 가능하다.
특히 스테로이드의 경우 장기간 사용할 경우 내성이 생겨 약효도 기대하기 어려운 상황이다. KLS-2031이 임상 절차를 넘어서면 최초 LSR 치료제로 인정받을 수 있는 셈이다.
관련 시장 규모도 빠르게 성장하고 있다. 시장분석 기관들에 따르면 2022년 35억1000만 달러(약4조8000억원) 규모였던 글로벌 신경조절 시장은 2030년까지 72억7000만 달러(약 10조원) 규모로 성장할 것으로 예상하고 있다. 이 기간 연평균 성장률(CAGR)은 9.59%에 달한다.
김선진 코오롱생명과학 대표이사는 앞서 보도자료를 통해 "KLS-2031은 신경병증성 통증 치료제가 절대적으로 부족한 의료계에서 미충족 의료 수요를 충족시킬 수 있는 신약개발 파이프라인으로서 중요한 의의를 가진다"며 "향후 후기 임상을 위한 RP2D 선정 등 후속 임상 개발과 함께 적응증 확대를 위한 전임상 시험도 동시에 수행해 나가겠다"고 밝혔다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- 이오플로우, 인슐렛 제기 'EU 판매금지' 소송 결론 도출
- [제약바이오 현장 in]제놀루션 "침체기 끝났다, 주력 3개 사업 2025년 변곡점"
- 인라이트벤처스, '위성 솔루션' 텔레픽스에 30억 '베팅'
- [매니저 프로파일/JB벤처스]유상훈 대표, 충청권 '로컬금융' 개척자 우뚝
- 새판 짜는 알파원인베, '운용정지' 펀드 정상화 '총력'
- 연 4% 금리 SC제일은행, '하이 통장' 첫선
- [i-point]바이오솔루션, 중국 하이난서 '카티라이프' 단독 강연
- [삼성·SK 메모리 레이스]하이닉스 대세론 '재확인', 300단대 낸드 조기 양산
- [클라우드 키플레이어 MSP 점검]안랩클라우드메이트, 공공시장 공략 전략 '네이버 동맹'
- 삼성전자, 10nm 미만 D램에 '핀펫' 도입






















