삼성바이오 美 상륙, 셀트리온에 답 있다 램시마와 유사 행보 '학습효과' 기대, 2018년 초 진출 전망
이석준 기자공개 2016-05-27 08:17:31
이 기사는 2016년 05월 25일 14:10 thebell 에 표출된 기사입니다.
삼성바이오에피스가 셀트리온에 이어 바이오시밀러 미국 허가에 도전한다. 삼성바이오에피스는 최근 셀트리온 '램시마'와 같은 성분(인플릭시맙, 오리지널 레미케이드)의 바이오시밀러 '렌플렉시스'에 대한 미국 승인 신청서를 제출했다.시장의 관심은 미국 허가 시점에 쏠려 있다. 임상 결과 데이터에는 큰 문제가 없어 보인다. 이미 국내 허가를 받았고, 유럽에서도 승인에 관한 긍정적인 의견을 받았기 때문이다.
|
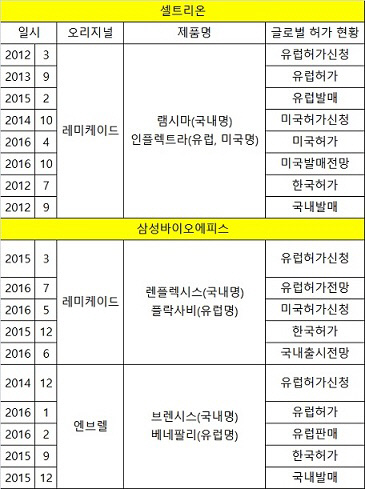
셀트리온은 삼성 바이오시밀러의 글로벌 허가 시기를 가늠할 수 있는 주요 예측인자다. 지난 4월 항체 바이오시밀러 최초로 미국 승인을 받고, 오는 10월 화이자와 판매를 계획 중인 셀트리온의 램시마(미국·유럽명 인플렉트라)는 렌플렉시스(유럽명 플락사비)의 선배나 다름없다. 렌플렉시스에 앞서 유럽과 국내는 물론 미국 시장에 먼저 안착했다.
시계를 거꾸로 돌려보자. 램시마는 지난 2012년 3월 유럽에서 허가 신청을 하고, 2013년 9월 승인을 받았다. 미국에서는 2014년 10월 승인 도전 후 올 4월 허가를 받았다. 유럽과 미국에서 허가를 받은 데 꼬박 1년 6개월이 소요된 셈이다.
렌플렉시스 역시 램시마와 비슷한 행보를 보일 것으로 예상된다. 유럽의 경우 오는 9월을 전후해 허가가 날 것으로 보인다. 지난해 3월 승인 신청을 했다는 점을 생각하면 램시마처럼 1년 6개월가량 지난 시점에 허가가 예상된다. 미국 허가는 2018년께 가능할 것으로 예상된다.
램시마에 대한 글로벌 학습 효과는 렌플렉시스의 유럽과 미국 승인 시점을 앞당기는 재료가 될 수 있다. 유럽에서 램시마는 오리지널 약제를 30% 대체할 정도로 처방이 크게 늘고 있다. 바이오시밀러 처방 필요성이 점차 부각되고 있다는 소리다. 이런 현상은 후발주자에게 큰 도움이 될 수 있다.
박상원 삼성바이오에피스 상무는 "지난 4월 이뤄진 램시마 미국 허가는 삼성 바이오시밀러 글로벌 진출에도 긍정적인 영향을 줄 것"이라며 "렌플렉시스 임상 3상에서 좋은 결과를 도출했다"고 강조했다.
업계 관계자는 "셀트리온의 앞선 행보를 보면 바이오에피스의 미래를 점칠 수 있다"며 "향후 양사는 과도한 경쟁을 지양하고 교차 처방 데이터 확보 등에서 근거를 쌓아 처방 영역 확대에 힘을 써야할 것"이라고 지적했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
best clicks
최신뉴스 in 전체기사
-
- 수은 공급망 펀드 출자사업 'IMM·한투·코스톤·파라투스' 선정
- 마크 로완 아폴로 회장 "제조업 르네상스 도래, 사모 크레딧 성장 지속"
- [IR Briefing]벡트, 2030년 5000억 매출 목표
- [i-point]'기술 드라이브' 신성이엔지, 올해 특허 취득 11건
- "최고가 거래 싹쓸이, 트로피에셋 자문 역량 '압도적'"
- KCGI대체운용, 투자운용4본부 신설…사세 확장
- 이지스운용, 상장리츠 투자 '그린ON1호' 조성
- 아이온운용, 부동산팀 구성…다각화 나선다
- 메리츠대체운용, 시흥2지구 개발 PF 펀드 '속전속결'
- 삼성SDS 급반등 두각…피어그룹 부담 완화