[국내 CAR-T 치료제 기업 동향]앱클론, 자체 개발 항체로 T세포 살상능력 높인다①작년 12월 식약처 임상 IND 승인...HK이노엔과 상업화 협업
홍숙 기자공개 2022-02-16 08:27:32
[편집자주]
킴리아, 예스카타, 브레얀지 등 글로벌 제약회사에서 품목허가를 받은 CAR-T 치료제 품목이 5종이다. 국내 기업들도 속속 다양한 차별화 전략으로 CAR-T 치료제 개발에 나서고 있다. 더벨은 국내에서 CAR-T 치료제 연구에 매진하고 있는 주요 기업들의 기술 및 생산 차별화 전략을 들어본다.
이 기사는 2022년 02월 15일 11:39 thebell 에 표출된 기사입니다.
"자체 개발한 항체 '1218'은 CD19에 효과적으로 결합해 T세포 살상능력을 더 높일 수 있는 항체다. 이 항체를 통해 보다 효과적인 CAR-T 치료제 개발에 나설 것이다."2010년 항체의약품과 CAR-T 치료제 개발을 위해 설립된 앱클론의 이종서 대표는 임상 1/2상에 진입한 ‘AT101’의 차별성에 대해 다음과 같이 말했다. 국내에서 킴리아가 품목허가를 받아 건강보험 급여 등재를 앞두고 있다.
여기에 큐로셀은 킴리아와 같은 적응으로 국내 기업 최초로 혈액암 CAR-T 치료제 임상에 진입했다. 같은 혈액암을 공략하는 앱클론은 지난해 12월 28일 식품의약품안전처로부터 AT101 임상시험계획(IND)을 승인받았다. 앱클론이 개발 속도면에서 뒤쳐져 있다는 인상을 주기도 한다. 하지만 이종서 앱클론 대표는 단호하게 AT101의 개발 속도가 늦은 것은 아니라고 말한다.
◇'1218' 항체로 DLBCL 외에 다양한 혈액암 공략할 것
CAR-T 치료제는 △암세포에 특이적인 항원을 인식할 수 있는 '항체'(세포외부위) △T세포를 활성화 시키는 역할을 하는 '세포자극부위' △암세포를 죽이는 T세포로 이뤄져 있다. 보통 혈액암을 치료하기 위해 품목허가를 받은 킴리아를 비롯한 대부분의 CAR-T 치료제는 'CD19'이라는 항원을 인식할 수 있는 항체를 사용한다.
이미 CD19을 인식하는 CAR-T 치료제는 킴리아와 예스카타를 비롯해 4가지가 품목허가를 받았다. 또 큐로셀 역시 CD19을 인식하는 CAR-T 치료제 임상 1상에 진행해 중간결과 분석을 발표했다. 앱클론은 1218 항체를 활용해 같은 CD19을 인식하더라도 차별화된 CAR-T 치료제 개발이 가능하다고 말한다. 특허 등록은 마친 자체 개발 항체 '1218'을 통해서다.
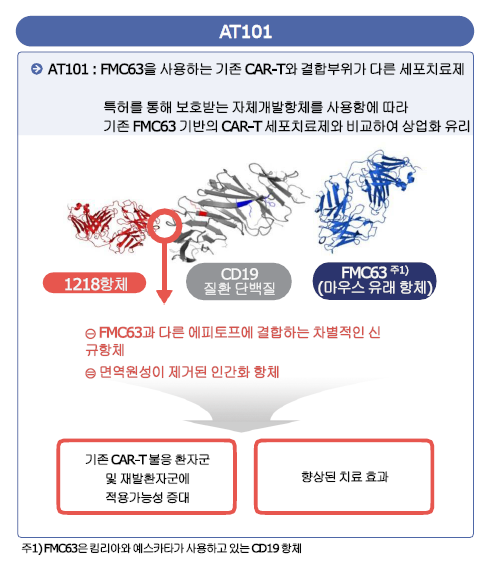
이종서 앱클론 대표는 "1218 항체는 킴리아 등 기존 CAR-T 치료제가 활용하는 FMC63 항체와 다른 에피토프에 결합하는 차별화된 물질"이라며 "이 항체를 활용하면 미만성거대B세포림프종(DLBCL) 외에도 다양한 유형의 혈액암 환자를 치료할 수 있을 것으로 기대한다"고 설명했다.
AT101이 진해하는 임상 1/2상은 비호지킨성 림프암 환자 80명을 대상을 진행된다. 1상은 코흐트 3개로 총 9명을 대상으로 독성 여부를 판별하는 과정이다. 이후 임상 2상 80명 내외로 서울아산병원을 포함해 다수의 의료기관과 진행한다.
이 대표는 "AT101 임상을 통해 킴리아 등 기존 CAR-T 치료제에 효과를 보이지 않은 환자를 아우를 수 있는 임상을 진행할 계획"이라며 "윤덕현 서울아산병원 교수를 임상책임자(PI)로 3월 첫 환자 모집(recruit)를 목표로 임상 절차를 진행 중"이라고 밝혔다.
앱클론은 임상 1상은 서울아산병원과 함께 올해 안으로 9명의 환자를 대상 조기 투여를 목표로 한다. 이후 임상 2상은 아산병원을 포함한 다수의 의료기관과 진행한다는 계획이다.

◇자동화 공정과 자체 임상시료 GMP 시설로 임상 속도 높일 것
킴리아 이후 CAR-T 치료제들은 이제 '자동화' 공정을 통해 생산에 나선다. 수작업으로 CAR-T 치료제의 생산 효율성을 낮추는 과정을 최소화하는 전략이다. 앱클론 역시 자동화 공정 기기를 활용해 연간 120명의 환자에게 제공할 수 있는 임상 시료용 GMP 시설을 구축했다.
그는 "앱클론은 회사 내 연간 환자 120명에게 투여할 수 있는 자체 임상시료용 GMP 시설을 갖추고 있다"며 "기존 킴리아와 예스카타 등이 제조 공정 상에서 실패를 해 생산성이 저하되는 부분이 있는데, 우리는 자동화 공정을 통해 약 2주만에 CAR-T 치료제 생산이 가능하다"고 말했다.
상업화를 위해선 HK이노엔과 손을 잡는다. 연구개발에 집중하기 위해서 향후 상업화를 위한 대량생산은 HK이노엔과 협업한다는 계획이다. 이를 위해 두 회사는 14일 AT101 공동개발을 위한 업무협약(MOU)를 맺었다. HK이노엔은 경기도 하남에 세포유전자치료제 개발을 위한 연구부터 임상시험약 제조, 상업용 치료제 생산까지 한번에 가능한 세포공장을 구축했다.
그는 "CAR-T 치료제 분야에서도 셀트리온과 삼성바이오로직스와 같이 대량 설비를 갖춘 대기업이 나오기 시작했다"며 "연구개발(R&D)에 집중해야 하는 벤처가 굳이 대량생산까지 운영(operation)하는 데는 한계가 있다"고 주장했다.
빠른 임상 진행을 위해서 임상시료 생산은 자체적으로 맡는다. 추후 대량생산을 위해서 HK이노엔과 협업을 통해 생산 효율화를 꾀한다는 계획이다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- 우리금융 "롯데손보 M&A, 과도한 가격 부담 안한다"
- 신한캐피탈, 지속성장 포트폴리오 리밸런싱 체계 강화
- 하나금융, ELS 악재에도 실적 선방…확고한 수익 기반
- 하나금융, 자본비율 하락에도 주주환원 강화 의지
- 국민연금, '역대 최대 1.5조' 출자사업 닻 올렸다
- [도전 직면한 하이브 멀티레이블]하이브, 강한 자율성 보장 '양날의 검' 됐나
- [퍼포먼스&스톡]꺾여버린 기세에…포스코홀딩스, '자사주 소각' 카드 재소환
- [퍼포먼스&스톡]LG엔솔 예견된 실적·주가 하락, 비용 절감 '집중'
- [퍼포먼스&스톡]포스코인터, 컨센서스 웃돌았지만 주가는 '주춤'
- 신한금융, ‘리딩금융’ 재탈환에 주주환원 강화 자신감




















