[클리니컬 리포트]지놈앤컴퍼니 GEN-001, 위암 '1차 치료' 순항'언멧니즈' 높은 3차에서 면역항암+마이크로바이옴 시너지
최은수 기자공개 2024-01-22 07:53:09
이 기사는 2024년 01월 19일 15:37 thebell 에 표출된 기사입니다.
지놈앤컴퍼니가 마이크로바이옴 치료제 GEN-001의 위암 2상에서 의미 있는 데이터를 공개했다. 면역항암제 처방이 제한적이던 위암에서 '마이크로바이옴 병용'을 위한 물꼬를 트기 위한 데이터를 확보했다는 평가다.무엇보다 이번 임상에서 가장 치료제 허들이 높은 위암 3차 치료제로의 포지셔닝 기대감을 더한 점이 눈길을 끈다. GEN-001은 위암 표준치료(1차 치료)로 진입하는 게 궁극적인 목표인데 이를 위한 긴 항해에서도 순풍을 만난 셈이다.
◇GEN-001, 위암 2상 컷오프서 인체 대상 통계적 유의성 확보
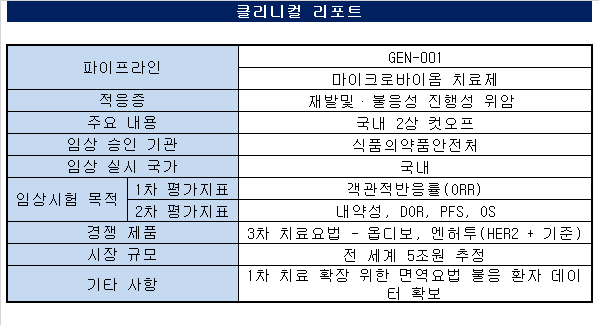
지놈앤컴퍼니는 통계적 유의성을 달성한 'GEN-001'의 위암 대상 임상 2상에 대한 컷오프 결과를 내놨다. GEN-001은 락토코커스 락티스 단일균주를 주성분으로 하는 경구용 마이크로바이옴 치료제다. 해당 데이터는 18일(미국 현지시간) 미국 임상종양학회 소화기암 심포지엄(ASCO GI)에서 포스터로 처음 발표됐다.
이번 데이터는 항암 치료에서 마이크로바이옴의 가능성을 보여준 첫 사례다. 이와 관련한 별도의 온라인 간담회를 열고 "마이크로바이옴이 장내에 장착한 마이크로바이옴이 위나 뇌 등 다른 부위에의 치료효과를 입증하는 건 과제였다"며 "마이크로바이옴 치료제 개발사 중 처음으로 '인체 대상' 위암에서 의미있는 데이터를 얻은 것"이라고 말했다.
배지수 대표(사진)는 이어 "세계적으로 다섯번째로 흔한 암이자 암 중 사망 원인 4위인 위암은 2차 치료 이상에 실패한 환자를 대상으로 한 위암 3차 치료제들의 성과가 낮고 미충족 의료수요가 높았다"며 "이번 결과로 병용 시 3차 치료제 이상에서 의미있는 생존기간 상향을 확인했다"고 말했다.
이번 2상에선 위암 2차 이상의 치료에 실패한 위암 또는 위식도 접합부 선종암 환자 42명에게서 'GEN-001'과 독일 머크의 면역항암제 '바벤시오'(성분명 아벨루맙)을 병용해, 3차 치료제로서의 가능성을 평가했다. 그 결과 부분반응(PR)이 7건으로, 객관적반응률(ORR) 16.7%였다.
기존 3차 치료제 대비 통계적으로 20%포인트 이상 개선된 데이터값이다. 특히 그간 허가를 얻어낸 3차 치료제가 낮은 객관적반응률로 의학적 미충족 수요(언멧니즈)가 크다는 평가를 받았는데 이를 대체할 가능성을 확인한 셈이다.
카플란 마이어 분석(Kaplan–Meier)을 통해 추정된 '무진행 생존기간'(질병 진행 없이 생존)의 중간값은 1.7개월, 전체생존기간(OS)의 중간값은 7.9개월이었다. 더불어 GEN-001이 유발한 심각한 안전성(Sevier, 카테고리 3) 부작용 사례는 보고되지 않은 점도 고무적이었다.
◇'3차 너머 1차·표준치료' 여타 면역항암제 병용 가능 실마리도 확보
주목할 부분은 기존에 면역항암제 투여를 받았으나 불응한 환자 8명 가운데 3명에서도 부분반응(객관적반응률 37.5%)을 얻은 점이다. 전체 위암 발병 모수를 살펴보면 아시아 지역이 75%를 차지한다. 다만 이 지역권에 효용성이 높은 치료 요법은 아직 명확하게 자리잡지 않았는데 GEN-001이 병용에서 이 '빈틈'을 잡을 실마리를 얻었다는 뜻이다.

이 상황에서 면역항암제 중심 치료 옵션이 계속 늘어나는 것도 주목할 부분이다. FDA는 2021년 4월 면역항암제 옵디보(Opdivo)와 세포독성항암제 병용요법을 승인했다. 다만 서양권 데이터를 중심으로 출시된 면역항암제의 경우 인종이나 유전 등의 이유로 아시아권에서 유효성이 높지 않은 경우가 있어 여전히 보완을 요구받는 중이다.
지놈앤컴퍼니가 이번 임상에서 확보한 면역항암제 불응성 환자(8명) 모수는 통계를 확보하기엔 다소 적다. 다만 각 환자의 무진행 생존기간은 5.6개월로 기존의 연구 결과의 베이스라인 대비 역시 30% 이상이 높은 점, 아직 생존자가 많아 전체생존기간 평균값을 도출하지 못한 것도 기대감을 높인다.
배 대표는 "그동안 면역항암제가 1차 치료제로 승인받은 만큼 변화한 시장에 맞춰 면역항암제 투여 환자 모집에 신경썼었다"며 "면역항암제를 보유하거나 병용치료에 관심있는 회사를 대상으로 폭넓은 사업화를 논의할 수 있을 것"이라고 기대했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- [루키 바이오텍 in market]지투지바이오, IPO 관전포인트 '매출안정성·특허이슈'
- [IR Briefing]HD현대인프라코어, 불황 속 더욱 빛난 '재무 체력'
- SK㈜, '머티리얼즈 퍼포먼스-에버텍' 흡수합병 결정
- [가이던스 달성률 분석]매출목표 내린 LG엔솔, 정확한 노선 수정
- [영풍-고려아연 경영권 분쟁]공개매수로만 3.2조 썼는데…뾰족한 수 없는 지분 차이
- [성장하는 인도 질주하는 현대차]“개발·생산·판매 미래전략, 현지화로 승부수”
- [성장하는 인도 질주하는 현대차]점증하는 리스크, HMIL 정공법으로 돌파
- 식약처, 큐로셀 '안발셀' 사전검토 착수…연내 허가 신청 예고
- [성장하는 인도 질주하는 현대차]기회의 땅 인도, 팽창하는 자동차시장
- [현대차그룹 뉴 글로벌 동맹]현대차-GM, 달랐던 헤리티지가 '연결고리'
최은수 기자의 다른 기사 보기
-
- [금융사 콜옵션 리뷰]KB금융, '이자보상배율' 탓 발행경쟁 대신 내실 선회
- [인벤토리 모니터]프레스티지바이오로직스, 수주 덕에 부활한 재고자산
- [금융사 콜옵션 리뷰]빅 이슈어 신한금융, 달라진 금리 환경 '미미한 영향'
- [2024 이사회 평가]'이사회 개선 난맥' 두산에너빌리티, 경영성과 하위권
- [2024 이사회 평가]'그룹 크레도' 따른 두산에너빌리티, 정보접근성 '양호'
- [2024 이사회 평가]두산에너빌리티, 취약한 견제·균형감에 낮은 총점
- [금융사 콜옵션 리뷰]여전히 높은 금리·고환율…복잡해진 계산법
- [2024 이사회 평가]'돈 버는 바이오' 셀트리온, 부채관리 '합격점'
- CJ그룹 '2인 CFO 실험'의 끝
- [2024 이사회 평가]셀트리온, 아쉬운 피드백 작업…시스템 개선 미흡

























