[i-point]제이엘케이, JLK-ICH 미 FDA 승인 획득두개내출혈 검출 솔루션…2025년 인허가 계획 순항 예고
김지원 기자공개 2025-01-06 10:52:49
이 기사는 2025년 01월 06일 10:52 thebell 에 표출된 기사입니다.
의료 AI 1호 상장기업 제이엘케이는 지난해 미국 FDA(식품의약국)에 인허가를 신청했던 JLK-ICH(두개내출혈 검출 솔루션)가 보완사항 없이 승인(FDA 510(k))을 획득했다고 6일 밝혔다.제이엘케이는 지난해 전립선암 솔루션 1개 획득에 이어 뇌졸중 솔루션에서만 3개 솔루션(JLK-LVO, JLK-CTP, JLK-PWI)의 승인을 획득했다. 이번 승인으로 제이엘케이는 뇌졸중 분야에서만 4개 솔루션에 대한 FDA 인허가를 확보하게 됐다.
특히 이번 인허가는 미국 FDA 별도 추가 보완 없이 단번에 승인받아 의미가 남다르다. 업계에서는 그동안 다수의 해외 인허가 진행으로 포트폴리오를 쌓아왔던 제이엘케이의 자체 인허가 역량이 인정받고 있다고 평가했다.
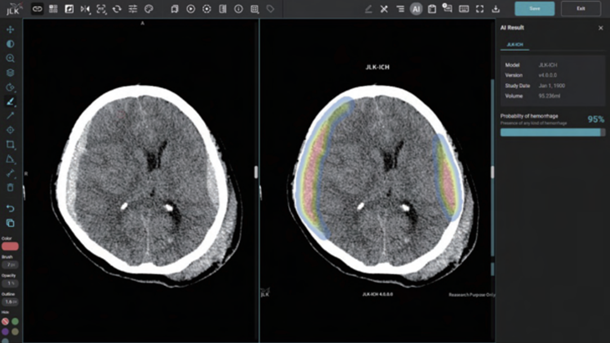
JLK-ICH는 제이엘케이가 주력하고 있는 뇌졸중 AI 솔루션으로 환자의 뇌 CT 영상을 분석해 뇌출혈 영역을 검출하는 AI 솔루션이다. 통상 뇌졸중 의심환자가 응급실에 도착하면 가장 먼저 뇌 CT를 촬영해 뇌출혈 여부를 확인하는데 이 과정에서 JLK-ICH가 빈번히 쓰일 것으로 예상된다. 기존에 획득한 JLK-LVO, JLK-CTP, JLK-PWI와 함께 연동돼 전주기에 걸친 뇌졸중 진단과 치료 결정 시 시너지를 낼 수 있을 것으로 기대된다.
혈관이 막히는 뇌경색 대비 중증도가 높은 뇌출혈은 출혈 크기 증가 우려와 재출혈 위험으로 치료까지 걸리는 시간을 단축하는 것이 환자 예후개선에 필수적이다. JLK-ICH는 임상연구를 통해 발생 특징이 다른 5가지 뇌출혈 유형에 대해 편차 없는 높은 검출 성능을 입증한 만큼 골든타임 확보에 큰 역할을 할 것으로 기대된다.
이번 FDA 승인으로 매출 확대를 위한 기반도 견고히 다졌다는 평가다. 미국의 연간 CT 촬상 수는 약 8600만 건에 이르러 CT 영상을 기반으로 하는 해당 솔루션의 미국 내 시장성이 높을 것으로 예상된다.
회사 관계자는 “지난해부터 글로벌 선진국 시장 진출을 위해 공격적으로 추진하고 있는 미국 FDA와 일본 PMDA 인허가 활동들이 빠른 결실을 맺고 있는 만큼 남은 솔루션들에 대한 인허가도 조속히 진행할 예정”이라고 전했다.
제이엘케이는 올해 인허가 신청과 승인 그리고 보험수가 획득에 집중해 해외 매출 확대의 포석을 마련한다는 목표를 세웠다. 올해 총 6개의 미국 FDA 인허가를 추가로 신청하고 8개 솔루션의 일본 PDMA 인허가 신청을 마친다는 계획이다.
김동민 제이엘케이 대표는 “JLK-ICH를 통해 올해 첫 해외 인허가 획득 소식을 전할 수 있어 기쁘다”며 “남은 인허가와 현지 보험수가 획득에 주력해 성공적인 해외 진출 성과를 거두기 위해 최선을 다하겠다”라고 말했다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
best clicks
최신뉴스 in 인더스트리
-
- [CES 2025]하정우 베어로보틱스 대표 "LG전자 동행 이어간다"
- [i-point]AP시스템, 잉여현금흐름·순이익의 30% 환원
- [Red & Blue]'V자 반등' HB테크놀러지, 유리기판 테마 효과
- [유동성 풍향계]세아제강지주, 자회사 투자부담에 '잉여현금' 급감
- [미트박스글로벌 road to IPO]두달만에 재도전, 뚝 떨어진 몸값
- [i-point]신테카바이오, 그린데이터센터 '플래티넘' 인증 획득
- 세라젬, CES 2년 연속 참가
- 코웨이, 넷마블 마브렉스 코인 699만개 보유
- 카카오엔터, 새 팬플랫폼 '베리즈'…디어유 시너지 주목
- [2025 승부수]'IPO 사활' SLL, 사업성 입증했지만…수익·재무 '넘을 산'
김지원 기자의 다른 기사 보기
-
- [i-point]제이엘케이, JLK-ICH 미 FDA 승인 획득
- [코스닥 CB 프리즘]'신규 조달' SCL사이언스, 사업 확대 드라이브
- [Red & Blue]'초전도체 사업' 본격화 신성델타테크, 주가 상승세 '지속'
- [i-point]제이엘케이, ‘의료 AI 허브 플랫폼’ 6번째 FDA 신청
- 금양인터내셔날, ‘마스트로베라르디노’ 출시
- [제주항공 여객기 사고]제주항공, 항공안전 투자비용은 늘려왔다
- [제주항공 여객기 사고]항공보험금 1.4조로 커버...요율 인상등 중장기 리스크
- 김이배 대표이사 "동계운항량 10~15% 감축"
- [2024 이사회 평가]HD현대마린엔진, 갈길 먼 이사회 경영
- [Company Watch]케이엔제이, 'SiC 링' 캐파 확대 속도
















