앱클론, CAR-T 첫 기술수출에 국내 허가 신청 예고까지 튀르키예 TCT에 'AT101' 현지 개발권 이전…국내외 개발 병행 전략 마련
김진호 기자공개 2025-03-05 09:13:35
이 기사는 2025년 03월 04일 16시20분 thebell에 표출된 기사입니다
앱클론이 키메릭항원수용체(CAR)-T 선도 물질 'AT101'에 대한 첫 기술수출 성과를 냈다. 계약 상대방은 튀르키예 신생 바이오텍이다.튀르키예 정부 지원으로 현지 시장 진출에 속도를 높인 다음 글로벌 시장 진출을 위한 거점으로 삼을 계획이다. 글로벌 개발이 탄력을 받을 수 있도록 올해 상반기 중 국내에서 AT101의 허가 신청도 완료한다는 방침이다.
◇튀르키예 'TCT'와 계약 체결, 패스트 트랙 개발 전략
앱클론은 4일 튀르키예 바이오텍 'TCT Health Technologies(TCT)'와 'AT101'에 대한 기술수출 계약을 체결했다고 공시했다. TCT에게 CD19 타깃 CAR-T 파이프라인인 AT101의 현지 개발 및 상업화를 위한 독점적 권리를 부여했다.
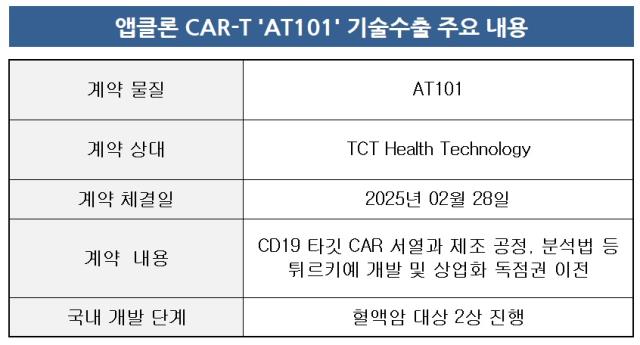
이번 계약에는 체결 후 60일 이내 지급해야 하는 선급급과 임상 진입에 따른 마일스톤, 상업화 성공 시 일정 비율의 경상기술료 등이 포함됐다. 계약 규모는 TCT의 요청에 따라 비공개다.
TCT는 'Heka Life Science'와 'Viscoran'이 합작해 2024년에 세운 바이오텍이다. 세포유전자치료제(CGT) 분야 혁신신약의 튀르키예 시장 도입을 앞당기는 것을 목표로 설립됐다. 작년 11월 지아이이노베이션과 NK세포 신약 파이프라인 관련 기술 수출 의향서를 체결한 데 이어 앱클론과 기술수출 계약을 추가로 맺게 됐다.
튀르키예 지역 내 AT101의 개발 비용은 모두 TCT가 부담하게 된다. 생산 공정은 싸이티바와 협력해 나갈 예정이다. TCT와 싸이티바, 앱클론 등 3사는 AT101의 생산을 위한 현지 GMP 시설을 올해 3분기 중 구축하는 것을 목표로 움직이고 있다. 튀르키예를 거점 삼아 EU와 중동 시장 진출도 병행해 나갈 계획이다.
이종서 앱클론 대표는 더벨과의 통화에서 "튀르키예 정부 차원에서 혁신적인 혈액암 치료제 도입을 앞당기려하고 있다"며 "1상 없이 AT101의 임상 2상부터 진입하는 등 패스트 트랙 개발 전략을 마련해 시도할 것"이라고 말했다.
◇CAR-T 불응 환자 대안 'AT101', 허가 신청 예고
글로벌 시장 진출의 첫발을 뗀 AT101는 국내 임상 2상도 연내 마무리될 것으로 기대된다. 앱클론은 임상 2상 중간 결과를 도출해 올 상반기 중 조건부 허가 신청에 나설 수 있다고 보고 있다.
AT101 임상 2상의 투약 목표인원은 82명이다. 앱클론은 약 40명의 투약 데이터를 바탕으로 중간 결과를 내놓는다는 계획이다. 2~3달 내로 결과를 공표하고 곧바로 허가 신청까지 진행한다는 구상이다.
효능과 약물 특수성 면에서 중간 결과로도 허가를 타진할 만한 데이터가 확보될 수 있다는 자신감이다. 무엇보다 기존 CAR-T에 불응한 환자에게 AT101을 적용할 수 있다는 점을 특장점으로 부각하려는 중이다.
스위스 노바티스의 '킴리아'나 미국 길리어드사이언스의 '예스카타' 등 글로벌 시장에는 이미 4종의 CD19 타깃 CAR-T가 시판돼 있다. 이들은 모두 CD19이라는 수용체의 FMC63이라는 부위(에피토프)와 결합하도록 설계됐다. 반면 AT101은 CD19에 있는 1218이라는 에피토프과 결합하도록 CAR를 발현시켰다.
이 대표는 "CAR-T 치료후 재발률은 40% 이상이다"며 "이런 환자에게 쓸 수 있는 대안이 AT101이다"고 말했다.
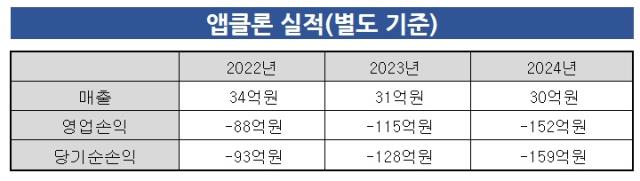
한편 앱클론은 AT101의 자체 임상 진행 과정에서 연구개발비가 늘면서 실적 부진을 겪어 왔다. 작년 매출 30억원이다. 전년 대비 1.9% 감소한 수치다. 영업손실은 152억원으로 2023년 115억원 보다 32.2% 증가했다.
연구개발비는 2022년 87억원, 2023년 107억원이었다. 작년 3분기 기준 연구개발비는 110억원으로 집계된 바 있다. 올해도 남은 임상 2상을 수행해야하는 만큼 연구개발비에 상당한 비용이 투입될 것으로 보인다.
< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
-
- [티엑스알로보틱스 road to IPO]고객사 2곳 비중 90%대, 높은 매출 의존도 '과제'
- [은행권 신지형도]디지털 경쟁력 척도 '플랫폼' 현황 살펴보니
- [NPL 플레이어 경쟁지도]우리금융F&I, 고속성장 후발주자…지주 혼란 속 전략은
- [저축은행 가계대출 총량규제 파장]태광 계열 예가람·고려저축, 중금리 대출 확장 '제동'
- [KB금융 CEO 인사이트]박찬용 KB데이타시스템 대표, "코어뱅킹 슬림화 등 그룹 전략 사업 리딩"
- [KB금융 CEO 인사이트]현대캐피탈, 글로벌 사업도 업계 선도…내수 부진에 성장 주춤
- 빈대인 BNK금융 회장의 '용병술'
- [KB금융 CEO 인사이트]이환주 KB국민은행장 "신뢰 회복이 최우선, 내부통제 혁신 추진"
- [저축은행 가계대출 총량규제 파장]'정책자금대출·중금리'도 포함...지주계 '직격탄'
- [금융지주 이사회 시스템 점검]사외이사 임기 관리에 '견제 기능' 달렸다
김진호 기자의 다른 기사 보기
-
- 앱클론, CAR-T 첫 기술수출에 국내 허가 신청 예고까지
- 엑셀세라퓨틱스 'MSC 배지' 미국 원료 인정에 신약도 등장
- [K-바이오 안질환 치료제 줌인]HLB테라, 임상 고배 '안구건조증' 연기…각막염으로 선회
- [K-바이오 안질환 치료제 줌인]한올바이오, 안구건조 세번째 도전 '허가까지 최소 5년'
- 쎌바이오텍, 힘 싣는 가족경영…창업주 딸 2인 '사내이사'
- 비보존제약 어나프라주 생산, 갑작스런 '생크션' 고민
- [K-바이오 안질환 치료제 줌인]질환 셋 '동시개발' 와이디생명…3상 진입한 안지오랩
- [K-바이오 안질환 치료제 줌인]큐라클, 이유있는 후기임상 도전 '경구제 시력개선' 유일
- 아리바이오 치매약 'AR1001' 미국 3상 환자 등록 완료
- 롯데바이오의 '솔루플렉스 링크', 오작동률 최소화 무기


























