[미지의 시장 '치매' 개화 길목에 서다]아리바이오 창업주가 던진 승부수 '52주 바이오마커'②정재준 대표 "약물 제형 매만지고 CRO도 직접 통제, 비용 절감 편견 아닌 '귀감'"
최은수 기자공개 2024-07-31 13:53:11
[편집자주]
인류 건강 최대 난제인 치매. 일라이릴리가 3번째 알츠하이머병 치료제 키썬라를 상업화 하면서 다시 한번 치매 시장에 대한 관심이 급부상하고 있다. 알츠하이머병으로 대표되는 치매 치료 '옵션'이 만들어졌지만 여전히 미지의 영역, 미완의 과제다. 더 많은 기업들의 공조 그리고 경쟁이 필요하다. 근본 치료 외 예방과 사후관리 등 시장의 '판'을 깨는 옵션도 눈여겨 볼 지점이다. 혁신신약 개발 기대주부터 진단과 사후 관리를 포함한 '치매 치료 전주기'를 노리는 기업들까지 더벨이 치매 시장을 들여다봤다.
이 기사는 2024년 07월 30일 08:57 thebell 에 표출된 기사입니다.
"질병과 관련한 바이오마커(생체표지자) 지표가 좋아지면 조건부 허가를 준다."미국 FDA는 올해 초 알츠하이머병과 관련해 새 임상 가이드라인을 내놨다. 인지기능 여부와 함께 '바이오마커 개선'을 핵심 지표로 부각시킨 게 요지다. 반면 '아밀로이드베타' 단백질 감소 기전은 주류에서 대리평가지표로 밀리며 여러 기업의 희비가 엇갈렸다.
아리바이오 창업주 정재준 대표(사진)은 이번 가이드라인으로 아리바이오의 AR1001 임상을 위한 최적 요건이 만들어졌단 입장이다. 아리바이오가 AR1001 투약기간을 통상 1년 반에서 '52주'로 단축한 점도 눈길을 끈다. 1250명 대상 3상 임상 기간을 줄여도 '바이오마커를 움직이는 걸 입증할 수 있다'는 자신감의 표현이다.
◇바이오마커 재평가와 PDE-5 메타분석도 '근본치료'로
그간 수 많은 신약개발기업은 알츠하이머병을 포함한 치매치료제 개발에 유독 난항을 겪었다. 이유는 뇌에 작용하기 위한 선행작업 즉 약물이 뇌를 보호하는 막인 뇌-혈관장벽(BBB)을 넘어가기 어려운 것과 '인지기능개선'이란 지표가 추상적이던 점에 있었다.
인류 건강 최대의 난제 항암 영역조차 임상적 의미(Clinical meaningfullness)를 확보하는 측면에선 '종양 크기'라는 명확한 지표가 존재한다. 그러나 알츠하이머병 및 치매는 다르다. 임상 지표가 모호하다는 것은 그만큼 약물 효능을 과학적으로 입증하기 어렵다는 의미다.
알츠하이머병이나 치매 외에도 파킨슨병이나 각종 비마약성 통증 치료제 역시 비슷한 상황에 있다. 정해진 수치로 객관화가 어려운 임상 지표를 요구하는 적응증일수록 시장을 지배하는 약물 출시가 늦어지고 개화도 오래 걸리는 이유다.
정 대표는 "AR1001의 임상 3상은 일반적 인지기능 지표인 임상치매등급척도-상자합계(CDR-SB) 외에도 뇌척수액(CSF)이나 혈장 등 다양한 바이오마커 변화를 관찰할 예정"이라며 "앞서 지표였던 인지기능 개선을 확인하기 위해 최소 18개월의 임상이 필요했지만 바이오마커 변화를 보려면 1년이면 충분하다"고 말했다.
AR1001가 타깃하는 크렙(CREB)·윈트(Wnt), 자가포식(Autophagy) 등 다중기전은 모두 바이오마커 변화로 입증이 가능한 영역이다. 이는 대표적인 발기부전 치료제 비아그라를 개발한 화이자나 씨알리스를 내놓은 일라이 일리도 주목하던 영역이다.
그럼에도 PDE-5 저해제가 결국엔 약물재창출에 해당하는 점과 다중기전이란 특성 그리고 바이오마커에 대한 인지도가 낮았던 점이 부정적인 상승효과를 냈다. 세계 각지에서 PDE-5 계열에 대한 긍정적인 메타분석 결과가 나왔지만 기존 학계에서 PDE-5 계열 약물과 AR1001를 증상 완화(Symtomatic) 즉 대증요법 정도로 평가절하했던 이유다.
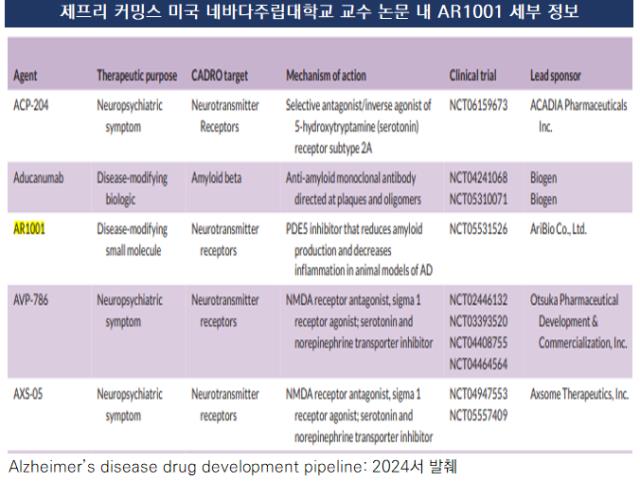
그러나 앞서 FDA 가이드라인 발표 후 학계에선 AR1001의 기전에 대한 괄목상대를 시작했다. 알츠하이머병 및 치매 치료에서 최고 권위자로 꼽히는 제프리 커밍스 교수도 최근 발표한 논문에서 AR1001을 병을 조절하는 저분자화합물, 즉 근본치료제(Disease Modifing Smallmolecule)로 새롭게 정의했다.
정 대표는 "앞서 FDA 가이드라인인 바이오마커 조절 여부에 따라 임상을 설계하면 1년 아니면 확실한 결과를 확인할 수 있다"며 "그 기간을 넘어서도 바이오마커 개선 효능이 나오지 않으면 임상은 실패한 것이라 오히려 투약 기간을 단축해 제시했고 인허가 기관의 승인도 얻었다"고 설명했다.
◇단가 낮추고 장기복용 전략…"제형·CRO·파트너십 전략 차별화"
정 대표는 앞서 유효성 입증을 위한 중요한 허들이 낮아진걸 고려해 이제는 아리바이오의 AR1001의 넥스트를 겨냥하고 있다. 가장 먼저 주안점을 두는 부분은 마케팅 및 약가 전략이다. 먼저 앞서 출시된 3개의 항체치료제가 모두 연간 2만5000달러(약 3500만원)이상의 약값을 요구하는 걸 유심히 보고 있다.
아리바이오는 AR1001의 약값을 저렴하게 책정하는 데 대한 부담이 상대적으로 크지 않다고 말한다. 이유는 AR1001이 비교적 저렴한 물질타입인 저분자화합물인 점과 함께 아리바이오 내부에서 철저한 '비용통제'가 있었기 때문이다. 임대료를 아끼기 위해 판교 외곽에 사옥을 구입하고 임상수탁기관(CRO)의 업무 일체를 직접 살펴보는 게 대표적이다.
정 대표는 "통상 CRO에 업무를 일임하는 턴키 계약을 지양하고 일체를 아리바이오 업무책임자가 들여다보고 피드백을 주고받는 구조를 꾸렸다"며 "나를 포함해 임직원들의 수고는 올라가지만 의외의 구간에서 재임상 이슈가 나타나고 추가 CRO 비용으로 겪는 재무적인 리스크나 난맥상을 없앨 수 있었다"고 말했다.
PDE-5가 이미 상당 부분 특허가 만료된 데 대한 경쟁기업 등장에 대한 우려도 높지 않다고 봤다. 아리바이오가 앞서 임상 기간을 52주로 줄이면서 당장 내년 말이면 최종데이터 분석을 위한 모든 절차가 마무리된다. 이르면 2026년 또는 2027년 상업화를 위한 절차를 밟을 수 있다.
정 대표는 "PDE-5로 알츠하이머병 치료제 개발을 노리는 후속기업과의 개발 격차는 7년 이상이 난다"며 "리브랜딩과 피보팅 이후 오로지 알츠하이머 혁신신약 하나를 향해 달려온 결과 아직 승인까지 관문은 넘었지만 여러 고비를 넘었고 어려울 때 회사를 지지하는 든든한 파트너도 생긴만큼 전망은 밝다"고 말했다.

< 저작권자 ⓒ 자본시장 미디어 'thebell', 무단 전재, 재배포 및 AI학습 이용 금지 >
관련기사
best clicks
최신뉴스 in 전체기사
최은수 기자의 다른 기사 보기
-
- [삼성의 CFO]'영업부터 재무까지 전천후' 이완삼 삼성생명 CFO
- [theBoard League Table]'바이오도 대기업이 하면 다르다' 최상위권 랭크
- [삼성의 CFO]'디지털 전환' 제일기획 안정감 더한 강우영 CFO
- [theBoard League Table]제약업계 거버넌스는 바이오에 비하면 '열등생'
- [theBoard League Table]삼성물산·삼성바이오 '공동 1위'…이사회도 '닮은꼴'
- [삼성의 CFO]삼성물산, '현재와 미래' 함께 만드는 재무라인
- [CFO change]토모큐브, CSO 맡은 구완성 상무 '재무총괄'까지
- [삼성의 CFO]삼성중공업, CFO 교체도 '슈퍼사이클 진입' 가리킨다
- [삼성의 CFO]'불확실 속 정중동 전략' 빛 본 김종성 삼성SDI 부사장
- [삼성의 CFO]'성숙기' 삼성바이오로직스, CFO '스코프'도 재정비






















